题目内容
【题目】必须加入还原剂才能实现的反应是( )
A.KCIO3 →O2B.Fe2+→ Fe3+C.SO2 →SD.CO32― →CO2
【答案】C
【解析】
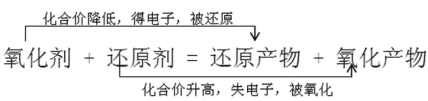
A.KCIO3 →O2,O元素的化合价从-2→0,化合价升高,被氧化,发生氧化反应,KCIO3作还原剂,所以必须加入氧化剂才能实现,A错误;
B. Fe2+→ Fe3+,Fe元素的化合价从+2→+3,化合价升高,被氧化,发生氧化反应,Fe2+作还原剂,所以必须加入氧化剂才能实现,B错误;
C. SO2 →S,S元素的化合价从+4→0,化合价降低,被还原,发生还原反应,SO2作氧化剂,所以必须加入还原剂才能实现,C正确;
D. CO32― →CO2,反应前后C、O元素的化合价都没变,不属于氧化还原反应。

【题目】将0.2 mol·L-1的KI溶液和0.05 mol·L-1 Fe2(SO4)3溶液等体积混合后,取混合液分别完成下列实验,能说明溶液中存在化学平衡“2Fe3++2I-![]() 2Fe2++I2”的是
2Fe2++I2”的是
实验编号 | 实验操作 | 实验现象 |
① | 滴入KSCN溶液 | 溶液变红色 |
② | 滴入AgNO3溶液 | 有黄色沉淀生成 |
③ | 滴入K3[Fe(CN)6]溶液 | 有蓝色沉淀生成 |
④ | 滴入淀粉溶液 | 溶液变蓝色 |
A. ①和②B. ②和④C. ③和④D. ①和③
【题目】类推思维是化学解题中常用的一种思维方法,下列有关反应方程式的类推正确的是
已知 | 类推 | |
A | 将Fe加入CuSO4溶液中Fe+Cu2+===Cu+Fe2+ | 将Na加入到CuSO4溶液中2Na+Cu2+===Cu+2Na+ |
B | 稀硫酸与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O | NaHSO4溶液与Ba(OH)2溶液反应至中性2H++SO42-+Ba2++2OH-===BaSO4↓+2H2O |
C | 铁和氯气反应2Fe+3Cl2 | 铁和碘单质反应2Fe+3I2 |
D | 向Ca(ClO)2溶液中通入少量CO2:Ca2++2ClO-+CO2+H2O===CaCO3↓+2HClO | 向Ca(ClO)2溶液中通入少量SO2:Ca2++2ClO-+SO2+H2O===CaSO3↓+2HClO |
A. A B. B C. C D. D