题目内容
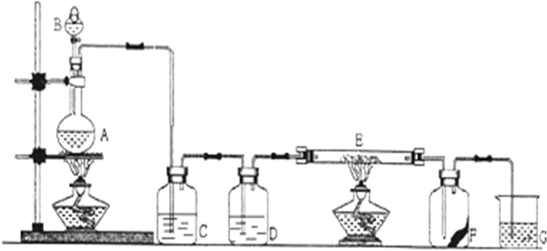
如图是实验室制取氯气并验证其性质的装置.C中装有饱和NaCl溶液,目的是除去氯气中的氯化氢杂质气体,E是中间装有铁丝网的硬质玻璃管.F是一张滴有KSCN和FeCl2混合溶液的滤纸.
试回答:
(1)仪器B的名称为 ;
(2)若用MnO2与浓盐酸共热制取Cl2,请写出相应的离子方程式 ;
(3)D的作用是 ;
(4)E中化学反应方程式为 ;
(5)请根据G的作用,写出G中的离子反应方程式 ;
(6)若F中滤纸变红,用离子反应方程式表示变红原因 ;
(7)将纯净的Cl2通入一定量石灰乳中来制取漂白粉,若通入224mL(标准状况下)Cl2完全反应,则反应过程中转移电子的物质的量为 .

试回答:
(1)仪器B的名称为
(2)若用MnO2与浓盐酸共热制取Cl2,请写出相应的离子方程式
(3)D的作用是
(4)E中化学反应方程式为
(5)请根据G的作用,写出G中的离子反应方程式
(6)若F中滤纸变红,用离子反应方程式表示变红原因
(7)将纯净的Cl2通入一定量石灰乳中来制取漂白粉,若通入224mL(标准状况下)Cl2完全反应,则反应过程中转移电子的物质的量为
考点:氯气的实验室制法
专题:实验题
分析:(1)根据常用化学仪器的名称、用途,进行分析解答即可;
(2)二氧化锰与浓盐酸反应生成氯气、氯化锰和水;
(3)发生装置制取的氯气中含有水蒸气,通入加热的E之前应进行干燥;
(4)氯气具有强的氧化性,能够与铁反应生成三氯化铁;
(5)氯气有毒,不能直接排放到空气中,可以用氢氧化钠溶液吸收;
(6)氯气具有强的氧化性,将二价铁离子氧化成三价铁离子,三价铁离子与KSCN呈现血红色;
(7)依据化学方程式电子守恒计算电子转移.
(2)二氧化锰与浓盐酸反应生成氯气、氯化锰和水;
(3)发生装置制取的氯气中含有水蒸气,通入加热的E之前应进行干燥;
(4)氯气具有强的氧化性,能够与铁反应生成三氯化铁;
(5)氯气有毒,不能直接排放到空气中,可以用氢氧化钠溶液吸收;
(6)氯气具有强的氧化性,将二价铁离子氧化成三价铁离子,三价铁离子与KSCN呈现血红色;
(7)依据化学方程式电子守恒计算电子转移.
解答:
解:(1)仪器B的名称为分液漏斗;故答案为:分液漏斗;
(2)MnO2与浓盐酸反应的离子方程式为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
故答案为:MnO2+4H++2Cl-
Mn2++Cl2↑+2H2O;
(3)D中盛放浓硫酸,用来除去从氯气中的水蒸气;
故答案为:干燥氯气;
(4)铁在氯气中点燃生成氯化铁,反应的化学方程式为:2Fe+3Cl2
2FeCl3;
故答案为:2Fe+3Cl2
2FeCl3;
(5)氯气有毒,不能直接排放到空气中,可以用氢氧化钠溶液吸收,反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(6)氯气氯气具有强的氧化性,将二价铁离子氧化成三价铁离子,反应的离子方程式为:Cl2+2Fe2+═2Cl-+2Fe3+,三价铁离子与KSCN呈现血红色;
故答案为:Cl2+2Fe2+═2Cl-+2Fe3+;
(7)氯气与石灰乳发生反应:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,Cl元素化合价从0价变化为-1价和+1价,消耗2mol氯气转移电子2mol,若通入224mL(标准状况下)Cl2,物质的量为0.01mol,完全反应转移电子0.01mol,
故答案为:0.01mol.
(2)MnO2与浓盐酸反应的离子方程式为:MnO2+4H++2Cl-
| ||
故答案为:MnO2+4H++2Cl-
| ||
(3)D中盛放浓硫酸,用来除去从氯气中的水蒸气;
故答案为:干燥氯气;
(4)铁在氯气中点燃生成氯化铁,反应的化学方程式为:2Fe+3Cl2
| ||
故答案为:2Fe+3Cl2
| ||
(5)氯气有毒,不能直接排放到空气中,可以用氢氧化钠溶液吸收,反应的离子方程式为:Cl2+2OH-=Cl-+ClO-+H2O;
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;
(6)氯气氯气具有强的氧化性,将二价铁离子氧化成三价铁离子,反应的离子方程式为:Cl2+2Fe2+═2Cl-+2Fe3+,三价铁离子与KSCN呈现血红色;
故答案为:Cl2+2Fe2+═2Cl-+2Fe3+;
(7)氯气与石灰乳发生反应:2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O,Cl元素化合价从0价变化为-1价和+1价,消耗2mol氯气转移电子2mol,若通入224mL(标准状况下)Cl2,物质的量为0.01mol,完全反应转移电子0.01mol,
故答案为:0.01mol.
点评:本题以氯气的制备为载体,考查了氯气的性质、离子方程式的书写、氧化还原反应的计算,题目综合性强,难度不大,依据所学知识不难解答.

练习册系列答案
 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
常温下,0.1mol的金属Na、Mg、Al分别投入到足量的稀盐酸中,完全反应后产生的氢气( )
| A、镁、铝一样多 |
| B、钠放出的多 |
| C、镁放出的多 |
| D、铝放出的多 |
月球土壤中含有较丰富的
He,在地球上氦元素主要以
He的形式存在,下列说法正确的是( )
| 3 |
| 2 |
| 4 |
| 2 |
A、
| ||||
B、
| ||||
C、
| ||||
D、
|