题目内容
14.某元素Y的核外电子数等于核内中子数,取2.8g该元素的单质与氧气充分反应,可得6.0g化合物YO2,则该元素在周期表中位置( )| A. | 第三周期ⅥA族 | B. | 第二周期ⅥA族 | C. | 第三周期ⅣA族 | D. | 第二周期ⅣA族 |
分析 2.8g该元素的单质与氧气充分反应,可得6.0g化合物YO2,则2.8g单质与3.2g氧气反应,n(O2)=$\frac{3.2g}{32g/mol}$=0.1mol,由R+O2=RO2可知,M(R)=$\frac{2.8g}{0.1mol}$=28g/mol,再结合核外电子数等于核内中子数来解答.
解答 解:2.8g该元素的单质与氧气充分反应,可得6.0g化合物YO2,则2.8g单质与3.2g氧气反应,n(O2)=$\frac{3.2g}{32g/mol}$=0.1mol,由R+O2=RO2可知,M(R)=$\frac{2.8g}{0.1mol}$=28g/mol,又核外电子数等于核内中子数,则质子数为14,为Si元素,位于元素周期表的第三周期ⅣA族,
故选C.
点评 本题考查元素周期表的结构及应用,把握物质的量的相关计算及R质子数的确定为解答的关键,侧重分析能力、计算能力的考查,题目难度不大.

练习册系列答案
相关题目
5. 目前已研制出一种用磺酸类质子作溶剂的酸性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )
目前已研制出一种用磺酸类质子作溶剂的酸性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )
 目前已研制出一种用磺酸类质子作溶剂的酸性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )
目前已研制出一种用磺酸类质子作溶剂的酸性乙醇电池,其效率比甲醇电池高出32倍,电池构造如图所示,电池反应式为:C2H5OH+3O2=2CO2+3H2O.下列关于该电池的说法正确的是( )| A. | 通入乙醇的电极为该电池的正极 | |
| B. | 电池工作过程中,H+从正极区向负极区迁移 | |
| C. | 该电池的正极反应为:4H++O2+4e-=2H2O | |
| D. | 每消耗0.1molC2H5OH,就会有0.6mole-经过导线 |
9.下表中括号内物质为所含的少量杂质,请选用适当的试剂和分离装置将杂质除去,并将所选的试剂及装置的编号填入表中.
试剂:①水 ②氢氧化钠 ③溴水 分离装置:A.分液装置 B.蒸馏装置 C.洗气装置 D过滤
试剂:①水 ②氢氧化钠 ③溴水 分离装置:A.分液装置 B.蒸馏装置 C.洗气装置 D过滤
| 需加入的试剂 | 分离装置 | |
| 苯(乙醇) | ||
| 乙烷(乙烯) | ||
| 乙醇(乙酸) | ||
| 溴苯(Br2) | ||
| 苯(苯酚) |
6.A、B、C三种短周期元素,A、B在同一周期,A、C的最低价离子分别为A2-、C-,离子半径A2-大于C-,B2+和 C-具有相同的电子层结构.下列判断正确的是( )
| A. | 原子序数由大到小的顺序是C>A>B | |
| B. | 原子最外层电子数由多到少的顺序是B>A>C | |
| C. | 离子半径由大到小的顺序是C->B2+>A2- | |
| D. | 原子半径由大到小的顺序是B>A>C |
3.σ键可由两个原子的s轨道、一个原子的s轨道和另一个原子的p轨道以及一个原子的p轨道和另一个原子的p轨道以“头碰头”方式重叠构建而成.则下列分子中的σ键是由两个原子的s、p轨道以“头碰头”方式重叠构建而成的是( )
| A. | H2 | B. | Cl2 | C. | NaCl | D. | HF |
4.下表为元素周期表的一部分,参照元素在表中的位置,请用化学用语回答下列问题:
(1)⑦的最低负价是-2;⑧的最高价含氧酸的化学式为HClO4.
(2)①和⑦两种元素的原子按1:1组成的常见化合物的电子式为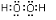 .
.
(3)③、④、⑦、⑧的简单离子半径由大到小的顺序为r (Cl-)>r (O2-)>r (Mg2+)>r (Al3+).
(4)⑤、⑥的单质中更易与①的单质反应的是N2,原因是氮的非金属性比碳强,因而其单质更易与氢气反应.
(5)②、④的最高价氧化物的水化物之间发生反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(6)用电子式表示③和⑨组成的化合物的形成过程 .
.
(7)海带中含有⑩元素,海带灰中含有该元素的简单阴离子,在硫酸酸化下,可用双氧水将其氧化为单质.写出该反应的离子方程式H2O2+2I-+2H+=I2+2H2O.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ⑤ | ⑥ | ⑦ | |||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑨ | |||||||
| 5 | ⑩ |
(2)①和⑦两种元素的原子按1:1组成的常见化合物的电子式为
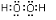 .
.(3)③、④、⑦、⑧的简单离子半径由大到小的顺序为r (Cl-)>r (O2-)>r (Mg2+)>r (Al3+).
(4)⑤、⑥的单质中更易与①的单质反应的是N2,原因是氮的非金属性比碳强,因而其单质更易与氢气反应.
(5)②、④的最高价氧化物的水化物之间发生反应的离子方程式:Al(OH)3+OH-=AlO2-+2H2O.
(6)用电子式表示③和⑨组成的化合物的形成过程
 .
.(7)海带中含有⑩元素,海带灰中含有该元素的简单阴离子,在硫酸酸化下,可用双氧水将其氧化为单质.写出该反应的离子方程式H2O2+2I-+2H+=I2+2H2O.