题目内容
【题目】难溶性杂卤石(K2SO4·MgSO4·2CaSO4·2H2O)属于“呆矿”,在水中存在如下平衡
![]()
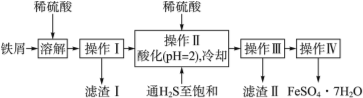
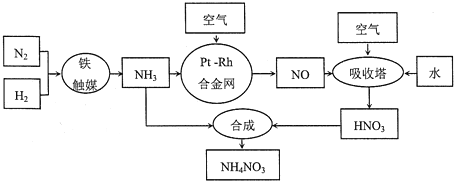
为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,工艺流程如下:

(1)滤渣主要成分有_______和_______以及未溶杂卤石。
(2)用化学平衡移动原理解释Ca(OH)2溶液能溶解杂卤石浸出K+的原因:
____ 。
(3)“除杂”环节中,先加入_______溶液,经搅拌等操作后,过滤,再加入_______溶液调滤液PH至中性。
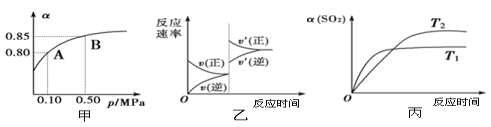
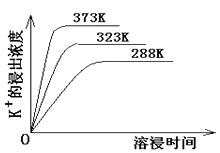
(4)不同温度下,K+的浸出浓度与溶浸时间的关系如下图,由图可得,随着温度升高,
①________________________②_______________
(5)有人以可溶性碳酸盐为溶浸剂,则溶浸过程中会发生:
![]() 已知298K时,Ksp(CaCO3)
已知298K时,Ksp(CaCO3)
=2.80×10-9,Ksp(CaSO4)=4.90×10-5,则此温度下该反应的平衡常数K为
(计算结果保留三位有效数字)。
【答案】(1)CaSO4;Mg(OH)2
(2)氢氧根与镁离子结合,使平衡向右移动,K+变多。
(3)K2CO3;H2SO4
(4)①在同一时间K+的浸出浓度大;②反应的速率加快,平衡时溶浸时间缩短。
(5)K=1.75×104
【解析】
试题分析:(1)“呆矿”,在水中存在沉淀溶解平衡:K2SO4MgSO42CaSO42H2O(s)2Ca2++2K++Mg2++4SO42-+2H2O,为能充分利用钾资源,用饱和Ca(OH)2溶液溶浸杂卤石制备硫酸钾,氢氧根离子和镁离子结合生成氢氧化镁沉淀,同时钙离子增多,析出硫酸钙沉淀,所以滤渣中主要成分为CaSO4,Mg(OH)2;
(2)加入Ca(OH)2溶液,OH-与Mg2+结合成Mg(OH)2、Ca2+与SO42-结合成CaSO4而析出,使平衡向右移动,杂卤石溶解浸出K+(留在滤液中)
(3))“除杂”环节主要是除去钙离子,依据除杂原则不能引入新的杂质,根据制取的目的是制备硫酸钾,所以加入的试剂易于除去,不引入新的杂质,因此加入过量K2CO3除钙离子,过滤后加入硫酸至中性,除去碳酸钾;
(4)分析不同温度下,K+的浸出浓度与溶浸时间的关系,温度越高K+的浸出浓度越大,溶浸时间越短,反应速率越大,达到平衡越快,故图象中分析得到的结论为:温度越高,在同一时间K+的浸出浓度大;反应速率加快,平衡时溶浸时间短
(5)溶浸过程中会发生:CaSO4(s)+CO32-(aq)CaCO3(s)+SO42-(aq),CaCO3(s)=Ca2++CO32-;CaSO4(s)=Ca2++SO42-;依据硫酸钙、碳酸钙溶度积常数的计算表达式,转化关系中钙离子相同计算,反应的平衡常数K= =1.75×104。
=1.75×104。

 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案