��Ŀ����
8���ߴ�̼�����ڵ��ӹ�ҵ������Ҫ��Ӧ�ã�ʪ���������̿���Ҫ�ɷ�ΪMnO2��������Fe��Al��Mg������Ԫ�أ��Ʊ��ߴ�̼���̵�ʵ��������£�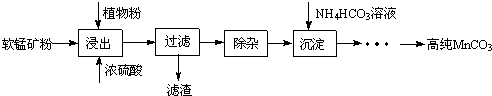
��1������������ʱ�¶ȿ�����90�桫95��֮�䣬����Ҫ��������3Сʱ��Ŀ����������̿����̵Ľ����ʣ�ֲ��۵�����������ԭ����
��2�����ӣ��������Һ�м���һ������̼���̿��ڽ���Һ��pHΪ3.5��5.5��
���ټ���һ���������̿��˫��ˮ�����ˣ�
�ۡ�
��������ʹ��̼���̵�pH������������MnCO3�IJ������������µ����ʵȣ����������м���˫��ˮ�����ܽ�Fe2+����ΪFe3+��������������̿�Ľ����ʣ�д��˫��ˮ������̿�����ʵ����ӷ���ʽMnO2+H2O2+2H+=Mn2++2H2O+O2����
��3���Ʊ�����30�桫35���£���̼�������Һ�μӵ������̾���Һ�У����Ʒ�ӦҺ������pH��6.5��7.0���õ�MnCO3�������¶ȿ���35�����µ�ԭ���Ǽ���̼����淋ķֽ⣬���ԭ�������ʣ��÷�Ӧ�Ļ�ѧ����ʽΪMnSO4+2NH4HCO3$\frac{\underline{\;30-35��\;}}{\;}$MnCO3 ��+��NH4��2SO4+CO2��+H2O�����ɵ�MnCO3�����辭���ϴ�ӣ�����ϴ���Ƿ���ȫ�ķ�����ȡ���һ�ε�ϴ����Һ1��2 mL ���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ���
��4�����㣺�����£�Ksp��MnCO3��=1.8��10-11��Ksp��MgCO3��=2.6��10-5����֪����Ũ��С��1.0��10-5mol•L-1ʱ����ʾ�����ӳ�����ȫ��������Һ�е�c��Mg2+��=10-2mol/L���Լ���˵��Mg2+�Ĵ����Ƿ��Ӱ��MnCO3�Ĵ��ȣ�
���� ʪ���������̿���Ҫ�ɷ�ΪMnO2��������Fe��Al��Mg������Ԫ�أ��Ʊ��ߴ�̼���̣�����Ũ�����ֲ��۽������˵õ���Һ��ȥ���ʣ�����̼������γɳ���ͨ��һϵ�в����õ��ߴ�̼���̣�
��1�����½��趼���Լӿ����ʵ��ܽⷴӦ���ʣ�����ֲ�����һ�ֻ�ԭ����
��2��ʹ��̼���̵�pH�������Dz������µ����ʣ���������������������Ϊ��������������ԭΪ�����ӣ�
��3������̼����������ֽ��������30�桫35���£���̼�������Һ�μӵ������̾���Һ�У����Ʒ�ӦҺ������pH��6.5��7.0���õ�MnCO3����������泥�������̼��ˮ�����ɵ�MnCO3�����辭���ϴ�ӣ�����ϴ���Ƿ���ȫ�ķ�����ȡ���һ��ϴ��Һ�����Ƿ��������������ƣ�
��4��Ksp ��MnCO3��=c��Mn2+��•c��CO32-������Mn2+������ȫʱ��c��CO32-��=1.8��10-11/1.0��10-5=1.8��10-6 mol•L-1����Mg2+Ҳ���γɳ�������Ҫ��Mg2+��2.6��10-5/1.8��10-6=14.4 mol•L-1��Mg2+��Ũ��0.01mol/LԶС��14.4 mol•L-1��
��� �⣺ʪ���������̿���Ҫ�ɷ�ΪMnO2��������Fe��Al��Mg������Ԫ�أ��Ʊ��ߴ�̼���̣�����Ũ�����ֲ��۽������˵õ���Һ��ȥ���ʣ�����̼������γɳ���ͨ��һϵ�в����õ��ߴ�̼���̣�
��1�����¡����趼���Լӿ����ʵ��ܽⷴӦ���ʣ�����ʱ�¶ȿ�����90�桫95��֮�䣬����Ҫ��������3Сʱ��Ŀ����������̿����̵Ľ����ʣ�����ֲ�����һ�ֻ�ԭ����
�ʴ�Ϊ��������̿����̵Ľ����ʣ�����ԭ����
��2��ʹ��̼���̵�pH�������Dz������µ����ʣ�������Һ�ж�������������������Ϊ��������������ԭΪ�����ӣ���Ӧ�����ӷ���ʽΪ��MnO2+H2O2+2H+=Mn2++2H2O+O2����
�ʴ�Ϊ������MnCO3�IJ������������µ����ʵȣ��� MnO2+H2O2+2H+=Mn2++2H2O+O2����
��3������̼����������ֽ�������¶ȿ���35�����µ�ԭ���Ƿ�ֹ̼����立ֽ⣬��30�桫35���£���̼�������Һ�μӵ������̾���Һ�У����Ʒ�ӦҺ������pH��6.5��7.0���õ�MnCO3����������泥�������̼��ˮ����Ӧ�Ļ�ѧ����ʽΪ��MnSO4+2NH4HCO3 $\frac{\underline{\;30-35��\;}}{\;}$ MnCO3+��NH4��2SO4+CO2��+H2O�����ɵ�MnCO3�����辭���ϴ�ӣ�����ϴ���Ƿ���ȫ�ķ�����ȡ���һ��ϴ��Һ�����Ƿ��������������ƣ�ȡ���һ�ε�ϴ����Һ1��2 mL ���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ���
�ʴ�Ϊ������̼����淋ķֽ⣬���ԭ�������ʣ�MnSO4+2NH4HCO3 $\frac{\underline{\;30-35��\;}}{\;}$ MnCO3+��NH4��2SO4+CO2��+H2O��ȡ���һ�ε�ϴ����Һ1��2 mL ���Թ��У������еμ��������ữ��BaCl2��Һ�����ް�ɫ�����������������ϴ�Ӹɾ���
��4��Ksp ��MnCO3��=c��Mn2+��•c��CO32-������Mn2+������ȫʱ��c��CO32-��=$\frac{1.8��1{0}^{-11}}{1.0}$��10-5=1.8��10-6 mol•L-1����Mg2+Ҳ���γɳ�������Ҫ��Mg2+��2.6��10-5/1.8��10-6=14.4 mol•L-1��Mg2+��Ũ��0.01mol/LԶС��14.4 mol•L-1��������Һ�е�c��Mg2+��=10-2mol/L��˵��Mg2+�Ĵ��ڲ���Ӱ��MnCO3�Ĵ��ȣ�
��Ksp ��MnCO3��=c��Mn2+��•c��CO32-������Mn2+������ȫʱ��c��CO32-��=$\frac{1.8��1{0}^{-11}}{1.0}$��10-5=1.8��10-6 mol•L-1����Mg2+Ҳ���γɳ�������Ҫ��Mg2+��2.6��10-5/1.8��10-6=14.4 mol•L-1��Mg2+��Ũ��0.01mol/LԶС��14.4 mol•L-1��������Һ�е�c��Mg2+��=10-2mol/L��˵��Mg2+�Ĵ��ڲ���Ӱ��MnCO3�Ĵ��ȣ�
���� ���⿼����������ᴿ���ۺ�Ӧ�ã�Ϊ��Ƶ���㣬�������̷������������뷽���������ķ�ӦΪ���Ĺؼ������ط�����ʵ�������Ŀ��飬��Ŀ�Ѷ��еȣ�

 Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д�
Ӯ�ڿ�����ʦ��ʱ�ƻ�ϵ�д� �������Ͽ�ʱͬ��ѵ��ϵ�д�
�������Ͽ�ʱͬ��ѵ��ϵ�д�| ѡ�� | ʵ�鷽�� | ���� | ���� |
| A | ��ˮ������ʢʳ���Թ��� | �����ݲ��� | ��������Ա�̼��ǿ |
| B | ��ʪ�����ɫ��ֽ����ij���� | ��ֽ��� | ���������������� |
| C | ��Na2CO3��Һ��ͨ��CO2 | �о������� | NaHCO3������ˮ |
| D | ���̪��Һ�м�����Na2O2 | ��Һ��� | Na2O2�Ǽ��������� |
| A�� | A | B�� | B | C�� | C | D�� | D |
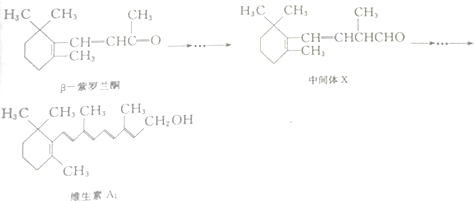
����˵����ȷ���ǣ�������
| A�� | ��-������ͪ�ں˴Ź�������ͼ����7��� | |
| B�� | ��-������ͪ���м���X��Ϊͬ���칹�� | |
| C�� | 1mol�м���X�������2mol H2�����ӳɷ�Ӧ | |
| D�� | ά����A1�ܷ���ȡ����Ӧ���ӳɷ�Ӧ��������Ӧ |
| A�� | �÷�Ӧ���ʱ�Ϊ��ֵ | |
| B�� | ���º����£�����ѹǿ��H2Ũ��һ����С | |
| C�� | �����¶ȣ��淴Ӧ���ʼ�С | |
| D�� | �÷�Ӧ��ѧ����ʽΪCO2��g��+H2��g�� $?_{����}^{����}$ CO��g��+H2O��g�� |
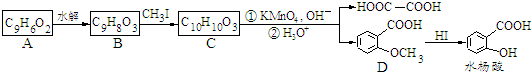
 ��
�� �ϳ�
�ϳ�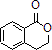 ��д����ػ�ѧ��Ӧ����ʽ
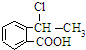
��д����ػ�ѧ��Ӧ����ʽ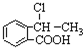 +NaOH$��_{��}^{��}$
+NaOH$��_{��}^{��}$ +H2O+NaCl��
+H2O+NaCl�� ��
��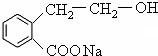 ++NaBr+H2O��2
++NaBr+H2O��2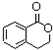 +2H2O+Na2SO4��
+2H2O+Na2SO4��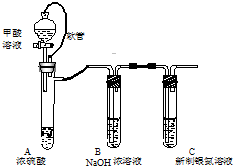 ������Һ�����ڼ��CO���壬ʵ�����о���װ����ͼ��
������Һ�����ڼ��CO���壬ʵ�����о���װ����ͼ��