题目内容
下面叙述中,正确的是( )
| A、硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位 |
| B、水泥是重要的硅酸盐产品,以纯碱、石灰石、二氧化硅为原料 |
| C、硅的化学性质不活泼,在自然界中可以以游离态存在 |
| D、硅是一种亲氧元素,在自然界中它总是与氧相互化合 |
考点:硅和二氧化硅,水泥的主要化学成分、生产原料及其用途
专题:碳族元素
分析:A.硅在地壳中的含量在所有的元素中居第二位;
B.水泥的原料有粘土、石灰石;
C.硅在自然界中以化合态存在;
D.硅是一种亲氧元素,在自然界中易二氧化硅和硅酸盐的形成存在.
B.水泥的原料有粘土、石灰石;
C.硅在自然界中以化合态存在;
D.硅是一种亲氧元素,在自然界中易二氧化硅和硅酸盐的形成存在.
解答:
解:A.硅在地壳中的含量在所有的元素中居第二位,仅次于氧,是构成矿物和岩石的主要元素,故A错误;
B.水泥的原料有粘土、石灰石,故B错误;
C.硅是一种亲氧元素,在自然界中以化合态存在,故C错误;
D.硅是一种亲氧元素,在自然界中易二氧化硅和硅酸盐的形成存在,故D正确.
故选D.
B.水泥的原料有粘土、石灰石,故B错误;
C.硅是一种亲氧元素,在自然界中以化合态存在,故C错误;
D.硅是一种亲氧元素,在自然界中易二氧化硅和硅酸盐的形成存在,故D正确.
故选D.
点评:本题主要硅及其化合物的性质与用途,为高频考点,侧重于元素化合物知识的综合理解和运用的考查,注意相关基础知识的积累,难度不大.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
除去下列溶液中的杂质(括号内是杂质)所用试剂不正确的是( )
| A、Fe(Al):用NaOH溶液 |
| B、NaCl溶液(Na2CO3):用盐酸 |
| C、K2SO4溶液(K2CO3):用H2SO4溶液 |
| D、NaCl溶液 (HCl):用AgNO3溶液 |
在组装原电池时,下列各项中不需要的是( )
| A、电极材料 | B、直流电源 |
| C、电解质溶液 | D、金属导线 |
设NA为阿伏加德罗常数的值,下列有关叙述正确的是( )
| A、11.2L O3气体中含有的氧原子数是1.5NA |
| B、含12.0g NaHSO4的水溶液中钠离子数为0.1NA |
| C、1mol OH-中电子数为10NA |
| D、每有1mol Cl2反应转移的电子数一定为2NA |
下列说法不正确的是( )
| A、青铜中含有的主要合金元素是锡和铅 |
| B、装运浓硫酸的铝罐车,在卸货后不能用水冲洗铝罐的内部 |
| C、半导体工业所说的“从沙滩到用户”是指将二氧化硅制成晶体硅 |
| D、氮的固定只有在高温、高压、催化剂的条件下才能实现 |
 向NaOH溶液中通入一定量CO2,结晶后得到白色固体,该白色固体配成溶液逐渐加入盐酸溶液(如图),则原白色固体的成分是( )
向NaOH溶液中通入一定量CO2,结晶后得到白色固体,该白色固体配成溶液逐渐加入盐酸溶液(如图),则原白色固体的成分是( )| A、NaOH和Na2CO3 |
| B、Na2CO3 |
| C、Na2CO3和NaHCO3 |
| D、NaHCO3 |
化学工业是国民经济的支柱产业,下列生产过程中不涉及氧化还原反应的是( )
| A、纯碱厂用侯氏制碱法制纯碱 |
| B、硝酸厂用氨氧化法制硝酸 |
| C、硫酸厂用接触法生产硫酸 |
| D、氮肥厂用氮气和氢气合成氨气 |
NA代表阿伏加德罗常数的数值,下列叙述正确的是( )
| A、在H2O2+Cl2=2HCl+O2反应中,每生成32g氧气,转移4NA个电子 |
| B、常温常压下,33.6L Cl2与56g Fe充分反应,转移电子数为3NA |
| C、标准状况下分子数为NA的CO、C2H4混合气体体积约为22.4L,质量为28g |
| D、在1L 0.2mol?L-1的硫酸铁溶液中含有的铁离子数为0.4NA |
下列说法正确的是( )
A、金属的晶胞如图所示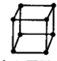 ,其配位数为8 ,其配位数为8 | ||||||||
| B、SO2分子中,S原子的价层电子对数为3,中心原子上孤电子对数为1,S原子为sp3杂化,是直线型分子 | ||||||||
| C、醋酸钠溶液中离子浓度的关系为:c(Na+)>c(CH3COO-)>c(H+)>c(OH-) | ||||||||
D、已知反应2CH3OH(g)?CH3OCH3+H2O(g),某温度下的平衡常数为400,此温度下,在恒容密闭容器中加入一定量CH3OH,某时刻测得各组分浓度如下表,则此时正、逆反应速率的大小关系为:v正>v逆
|