题目内容
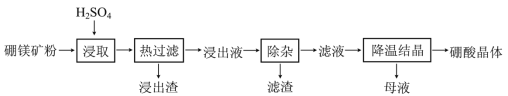
【题目】硼酸(H3BO3)大量应用于玻璃制造行业,以硼镁矿(含2MgO·B2O3·H2O、SiO2及少量Fe3O4、CaCO3、Al2O3)为原料生产硼酸的工艺流程如下:
已知:H3BO3在20℃、40℃、60℃、100℃时的溶解度依次为5.0 g、8.7 g、14.8 g、40.2g。Fe3+、Al3+、Fe2+和Mg2+以氢氧化物形式完全沉淀时,溶液的pH分别为3.2、5.2、9.7和12.4。
(1)“浸取”时主要反应的化学方程式为_____________________。
(2)“浸取”后,采用“热过滤”的目的是___________________________。
(3)“浸出液”显酸性,含H3BO3和Mg2+、SO42-,还含有其他杂质。“除杂”时向浸出液中依次加入适量H2O2和MgO,除去的杂质离子是__________。H2O2的作用是______(用离子方程式表示)。
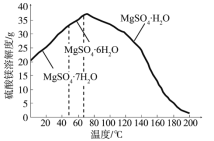
(4)“母液”可用于回收硫酸镁,已知硫酸镁的溶解度随温度变化的曲线如图,且溶液的沸点随压强增大而升高。为了从“母液”中充分回收MgSO4H2O,应采取的措施是将“母液”蒸发浓缩后,最佳结晶条件是_____________。
A. 升温结晶 B. 降温结晶 C. 加压升温结晶 D. 降压降温结晶
(5)在实际生产中为了提高原料的综合利用率,可以利用除杂后滤渣作为提炼铝的原料,工艺流程为:
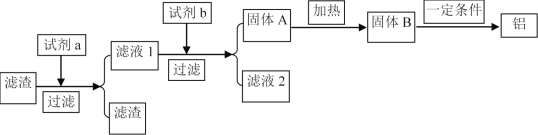
试剂a可选用________(化学式)溶液,若试剂b为AlCl3则由滤液得固体A的离子反应方程式为___________,在实际工业生产中,流程中的一定条件指的是________。
【答案】2MgOB2O3H2O+2H2SO4=2H3BO3+2MgSO4 防止温度下降时H3BO3从溶液中析出 Fe3+、Fe2+、Al3+ H2O2 + 2H+ +2Fe2+ = 2Fe3+ + 2H2O C NaOH Al3++3AlO2-+6H2O=4Al(OH)3↓ 熔融电解
【解析】
由流程可知,加硫酸溶解只有SiO2不溶,CaO转化为微溶于水的CaSO4,趁热过滤,防止H3BO3从溶液中析出,“除杂”需先加H2O2溶液,将亚铁离子转化为铁离子,再加入MgO调节溶液的pH约为5.2,使铁离子、铝离子均转化为沉淀,则滤渣为氢氧化铝、氢氧化铁,然后蒸发浓缩、冷却结晶、过滤分离出H3BO3,
(1)根据元素守恒可写出2MgO·B2O3·H2O浸取生成H3BO3的化学方程式;
(2)由目信息可知:H3BO3的溶解度随温度的升高而增大,所以要采用“热过滤”,以防温度下降时H3BO3从溶液中析出,加硫酸溶解只有SiO2不溶,CaO转化为微溶于水的CaSO4;
(3)浸出液中有 Fe3+、Fe2+、Al3+杂质,通过调节溶液pH值除去杂质且不引入新的杂质,H2O2将Fe2+氧化成Fe3+,反应的离子方程式是H2O2 + 2H+ +2Fe2+ = 2Fe3+ + 2H2O ;
(4)根据MgSO4.H2O的溶解度随温度变化的曲线可知,温度越高,MgSO4.H2O溶解度越小,据此判断操作;
(5) 滤渣是氢氧化铁和氢氧化铝,加入氢氧化钠溶液,氢氧化铝与氢氧化钠反应生成偏铝酸钠和水,滤渣是氢氧化铁,向偏铝酸钠溶液中通入二氧化碳或者氯化铝溶液生成氢氧化铝沉淀,过滤得到氢氧化铝,加热氢氧化铝分解得到三氧化铝和水,电解熔融氧化铝制得铝。
(1)根据元素守恒可写知2MgO·B2O3·H2O浸取生成H3BO3的化学方程式为2MgOB2O3H2O+2H2SO4=2H3BO3+2MgSO4 ,
故答案为:2MgOB2O3H2O+2H2SO4=2H3BO3+2MgSO4 ;
(2)浸出液中有 Fe3+、Fe2+、Al3+杂质,需要通过调节溶液pH值除去杂质且不引入新的杂质,所以加入MgO调节溶液pH的目的是除去溶液中的 Fe3+、Fe2+、Al3+杂质,H2O2将Fe2+氧化成Fe3+,反应的离子方程式是H2O2 + 2H+ +2Fe2+ = 2Fe3+ + 2H2O,
故答案为:除去溶液中的 Fe3+、Fe2+、Al3+杂质;H2O2 + 2H+ +2Fe2+ = 2Fe3+ + 2H2O ;
(3)由题目信息可知:H3BO3的溶解度随温度的升高而增大,所以要采用“热过滤”,以防温度下降时H3BO3从溶液中析出,
故答案为:防止温度下降时H3BO3从溶液中析出;
(4)根据MgSO4H2O的溶解度随温度变化的曲线可知,温度越高,MgSO4H2O溶解度越小,所以从“母液”中充分回收MgSO4H2O,应采取加压升温结晶的方法,
故选:C;
(5)滤渣是氢氧化铁和氢氧化铝,加入氢氧化钠溶液,氢氧化铝与氢氧化钠反应生成偏铝酸钠和水,滤渣是氢氧化铁,向偏铝酸钠溶液中通入二氧化碳或者氯化铝溶液生成氢氧化铝沉淀,加入氯化铝发生反应的离子方程式是:Al3++3AlO2-+6H2O=4Al(OH)3 ↓,过滤得到氢氧化铝, 加热氢氧化铝分解得到氧化铝和水,电解熔融氧化铝制得铝,
故答案为: NaOH;Al3++3AlO2-+6H2O=4Al(OH)3↓;熔融电解。

 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案