题目内容
【题目】铝土矿(主要成分为Al2O3,还含有SiO2、Fe2O3)是工业上制备金属铝的主要原料.工业上提取铝的工艺流程如下:
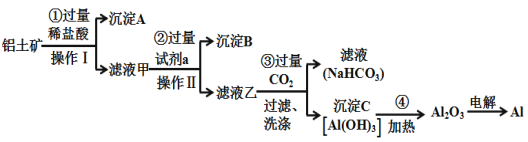
(1)沉淀A的化学式是____,沉淀B的化学式是____,滤液甲中所含金属离子是___、____,试剂a的化学式为__________;
(2)步骤③中通入过量CO2,产生沉淀C的离子方程式为___________________________________;
(3)Al2O3中所含的化学键的类型为________________;
(4)工业上用电解熔融Al2O3的方法制备金属铝,其反应方程式为_____________________________;
(5)在生活中,常利用Al与Fe2O3间的铝热反应来进行焊接钢轨。除了Fe2O3,铝粉还可以与很多金属氧化物组成铝热剂,下列氧化物中不能与铝粉组成铝热剂的是(___________)
a.MgO b.V2O5 c.Fe3O4 d.MnO2
【答案】SiO2 Fe(OH)3 Fe3+ Al3+ NaOH AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-或 [Al(OH)4]-+CO2=Al(OH)3↓+HCO3- 离子键 2Al2O3![]() 4Al+3O2↑ a
4Al+3O2↑ a
【解析】
铝土矿主要成分为Al2O3,还含有SiO2、Fe2O3,铝土矿中加入过量试剂盐酸,Al2O3 、Fe2O3可以溶解,SiO2不溶,所以沉淀A为SiO2;滤液甲中有Al3+、Fe3+和过量的H+,加入过量NaOH溶液后,Al3+会转化为AlO2-,Fe3+会转化为Fe(OH)3沉淀。过滤后得到滤液乙中含有NaAlO2,再通入过量的CO2,又会得到沉淀C为Al(OH)3,加热后得到Al2O3,再冶炼得到金属Al,据此分析作答。
(1)结合上述分析可知:因为Al2O3、Fe2O3可以溶解于盐酸,而SiO2不溶与盐酸,所以沉淀A为SiO2;滤液甲中有金属离子Al3+、Fe3+和过量的H+,根据Fe3+和Al3+性质,要除去Fe3+,保留Al3+,应加入NaOH溶液,所以试剂a为NaOH溶液,其化学式为NaOH;所得的沉淀B为Fe(OH)3,所以答案:SiO2;Fe(OH)3;Fe3+、Al3+;NaOH;
(2)根据上述分析可知滤液乙为NaAlO2,步骤③中通入过量CO2,得到的沉淀C为Al(OH)3,产生沉淀C的离子方程式为:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-或 [Al(OH)4]-+CO2=Al(OH)3↓+HCO3-;
(3)Al2O3为离子化合物,所以Al2O3中所含的化学键的类型为离子键,故答案为:离子键;
(4)工业上电解熔融Al2O3生成金属铝和氧气,其反应的方程式为:2Al2O3![]() 4Al+3O2↑
4Al+3O2↑
(5)铝热反应是利用了铝的还原性,铝能置换出活泼性较铝弱的金属,镁的金属性比铝强,所以铝不能置换出镁,本题正确答案是a。

 轻松暑假总复习系列答案
轻松暑假总复习系列答案【题目】Ⅰ.室温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略混合后溶液的体积变化),实验数据如下表:
实验序号 | 起始浓度/(mol·L-1) | 反应后溶液的pH | |
c(HA) | c(KOH) | ||
① | 0.1 | 0.1 | 9 |
② | x | 0.2 | 7 |
请回答:
(1)HA溶液和KOH溶液反应的离子方程式为_____。
(2)下列关于反应后的溶液说法不正确的是____(填字母)。
a.实验②反应后溶液中只存在着两个平衡
b.实验②反应后溶液中:c(A-)+c(HA)>0.1mol·L-1
c.实验②反应后溶液中:c(K+)=c(A-)>c(OH-)=c(H+)
d. 实验①反应后的溶液中由水电离出的c(OH-)=10-9mol·L-1;x>0.2mol·L-1
Ⅱ.已知2H2(g)+O2(g)=2H2O(1) ΔH=-572kJ·mol-1。某氢氧燃料电池以疏松多孔石墨棒为电极,KOH溶液为电解质溶液。
(3)写出该电池工作时负极的电极反应式____。
(4)若该氢氧燃料电池每释放228.8kJ电能时,会生成1mol液态水,则该电池的能量转化率为____。