题目内容
【题目】亚氯酸钠(NaClO2)是一种重要的消毒剂,主要用于水、砂糖、油脂的漂白与杀菌。以下是制取亚氯酸钠的工艺流程:
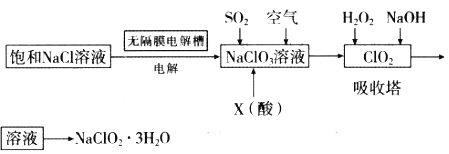
已知:①NaClO2的溶解度随着温度升高而增大,适当条件下可结晶析出。
②ClO2气体在中性和碱性溶液中不能稳定存在。
回答下列问题:
(1)用于电解的食盐水需先除去其中的Ca2+、Mg2+、SO42-等杂质。除杂操作时,往粗盐水中先加入过量的_________(填化学式),至沉淀不再产生后。再加入过里的Na2CO3和NaOH,充分反应后将沉淀一并滤去。在无隔膜电解槽中用惰性电极电解一段时间生成NaClO3,阳极反应式为_______
(2)X酸是_________。写出二氧化氯发生器中生成ClO2的化学方程式_______,吸收塔内的温度不宜过高的原因为________
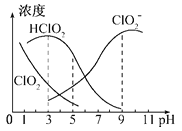
(3)亚氯酸钠在溶液中可生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都具有漂白作用,但ClO2有毒,经测定,25℃时各组分含量随pH变化情况如图所示(Cl-没有画出)。则下列分析正确的是(_____)
A.亚氯酸钠在碱性条件下较稳定
B.25℃时,HClO2的浓度随PH增大而增大
C.PH=6时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-)
D. 25℃时,该溶液在pH=4时比pH=2时更适合漂白
(4)aKg 30%的双氧水理论上可最多制得___Kg NaClO2·3H2O
【答案】 BaCl2 Cl-+6OH--6e-=ClO3-+3H2O 硫酸 2NaClO3+SO2=Na2SO4+2ClO2 防止H2O2分解 AD 2.55a
【解析】(1)加入过量的Na2CO3和NaOH,可分别除去Ca2+、Mg2+,在除杂的过程中每步加入的试剂必须是过量的,使离子除尽;过量的离子在下一步中必须出去,故先加入BaCl2,除去硫酸根,过量的钡离子,加入Na2CO3除去;电解池中阳极失去电子,所以溶液中的氯离子在阳极失去电子,因此反应的电极反应式是Cl--6e-+6OH-=ClO3-+3H2O;
(2)由于ClO2气体在中性和碱性溶液中不能稳定存在,所以只能在酸性环境中存在,由于在酸性条件下,氯酸钠容易和盐酸发生氧化还原反应,所以X应该是硫酸;发生器中NaClO3和SO2生成ClO2和Na2SO4,此反应的化学方程式为2NaClO3+SO2=Na2SO4+2ClO2 ,H2O2不稳定,温度过高,H2O2容易分解,吸收塔的温度不能过高,其目的是防止H2O2分解;
(3)A.由图可以得出:碱性条件下ClO2-浓度高,即在碱性条件下亚氯酸钠较稳定,故A正确;B.由图示可知25℃时,当溶液pH=3后,HClO2的浓度随PH增大而减小,故B错误;C.根据图知,pH=6时,存在c(HClO2)=c( ClO2-),故C错误;D. HClO2是漂白织物的有效成分,ClO2是有毒气体,要使漂白剂的漂白性强,即HClO2的含量高,又要使ClO2浓度较小,根据图象知,pH过小,ClO2含量较大,pH过大,HClO2的含量较低,当溶液的pH为4.0~4.5时二者兼顾,即为使用该漂白剂的最佳pH,应该是4-5,故D正确;答案为AD。
(4)设理论生成NaClO23H2O的质量为m,则
H2O2~2ClO2-~2NaClO23H2O
34289
akg×30% m
m=![]() =2.55akg。
=2.55akg。