题目内容
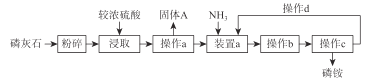
【题目】以磷灰石(一类含钙的磷酸盐矿物总称)原料生产磷铵的工艺流程图如下:
已知:纯的磷酸铵盐为白色晶体,其中以磷酸一铵最稳定,磷酸二铵次之,磷酸三铵不稳定,不宜作肥料使用。
(1)用硫酸浸取磷灰石,利用了硫酸的__________等性质。
(2)操作 a 的名称是__________;装置a中要控制“N/P”,使反应能生成较多的一种酸式盐,其化学式为__________。
(3)固体 A 的化学式为__________,其用途有__________。
(4)操作b为__________、__________。
(5)磷铵属于________。 (填写“单一”或“复合”)
(6)操作C为过滤、洗涤、干燥,在洗涤过程中可选用下列试剂进行洗涤________ (选填字母),其优点是________。
(7)本工艺流程中操作 d 的目的是________。
【答案】(1)难挥发性、强酸性 (2)过滤 NH4H2PO4 (3)CaSO4·2H2O 生产石膏
(4)蒸发浓缩、冷却结晶 (5)复合 (6)A 既能洗去可溶性杂质,又能降低产品的溶解损耗(NH4)2SO4 (7)循环利用滤液,提高原料的利用率
【解析】
试题分析:(1)由于硫酸具有难挥发性和强酸性,故可以用硫酸浸取磷灰石制取磷酸。(2)浸取液中有磷酸和CaSO4·2H2O固体,通过过滤将其分离;根据信息,控制“N/ P”比,使反应生成最稳定的磷酸—铵(NH 4H2PO4 )。(3)根据过滤(操作a)所得固体A为CaSO4·2H2O,可用于生产石膏。(4)从溶液中提取可溶性盐的—般操作为蒸发浓缩、冷却结晶、过滤、洗涤、干燥等。(5)NH4H2PO4中含有氮、磷元素,属于复合肥。(6)用自来水、硫酸、氨水洗涤均增加产品中的杂质,用冷的纯水洗涤。既能洗去可溶性杂质,又能降低产品的溶解损耗;由于反应液中混有SO42-,故产品中的主要杂质为(NH4)2SO4。(7)通过操作C,分离出磷铵晶体后的滤液和洗涤液均含有 NH4H2PO4,最后通过操作d循环利用,能大大提高原料的利用率。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】短周期元素 W、X、Y、Z 在元素周期表中的位置如右图所示。其中 Z 的单质是一种重要半导体材料,广泛应用于电子工业的各个领域。
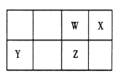
(1)W 在元素周期表中的位置是____________。
(2)W、X、氢元素形成的三原子分子的电子式____________。
(3)下列选项中,能证明元素非金属性X强于W的是____________。
A.相对原子质量:X>W | B.最低化合价:X>W |
C.最简单氢化物的稳定性:X>W | D.最高价氧化物的水化物酸性:X>W |
(4)元素周期表中与 Z 同周期的某金属元素形成的单质 A,可发生如下图所示的转化:

其中化合物D是一种白色沉淀,则 B 中溶质的化学式为____________;
B与 C也可直接转化生成 D 写出对应的离子方程式为____________。