题目内容
4.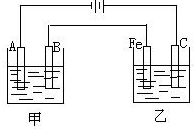 如图,甲、乙为相互串联的两个电解池,请回答下列问题:
如图,甲、乙为相互串联的两个电解池,请回答下列问题:(1)若甲池为用电解原理精炼铜的装置,则A电极名称为阴极,电极材料是精铜,(粗铜还是精铜).电极反应式是Cu2++2e-=Cu
(2)若乙池中是饱和食盐水(滴有少量酚酞试液),开始电解后,铁极附近呈红色,乙池中铁极上发生的电极反应式为2H++2e-=H2↑.
分析 图示是两个串联的电解池,依据电源判断A为阴极,B为阳极,Fe为阴极,C为阳极;
(1)依据电解原理精炼铜的装置是粗铜做阳极,精铜做阴极;含铜离子的溶液做电解质溶液;
(2)乙池中是电解饱和食盐水,溶液中的氢离子在阴极得到电子发生还原反应生成氢气,破坏了水的电离平衡,氢氧根离子浓度增大;
解答 解:图示是两个串联的电解池,依据电源判断A为阴极,B为阳极,Fe为阴极,C为阳极;
(1)依据电解原理精炼铜的装置是粗铜做阳极,精铜做阴极;含铜离子的溶液做电解质溶液;所以A极是阴极;材料是精铜;电极反应为:Cu2++2e-=Cu;B为阳极;材料是粗铜;电极反应主要为:Cu-2e-=Cu2+;电解质溶液是CuSO4溶液;
故答案为:阴;精铜;Cu2++2e-=Cu;
(2)乙池中是电解饱和食盐水,溶液中的氢离子在阴极得到电子发生还原反应生成氢气,破坏了水的电离平衡,氢氧根离子浓度增大,遇酚酞变红,即Fe电极附近变红;
故答案为:红;2H++2e-=H2↑.
点评 本题考查了电解池的工作原理的应用,电极判断方法,电极反应的书写,串联的电解池,电极的分析判断,难度不大.

练习册系列答案
相关题目
14.N2O5是一种新型硝化剂,在一定温度下可发生下列反应:2N2O5(g)?4NO2(g)+O2(g)△H>0;一定温度下,向10L恒容密闭容器中通入N2O5,的部分实验数据见下表:下列说法不正确的是( )
| t/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/mol | 5.00 | 3.5 | 2.50 | 2.50 |
| A. | 500 s内N2O5分解速率为3×10-4mol•(L•s)-1 | |
| B. | 反应达平衡后,往容器中加入5molN2O5气体,平衡正向移动,反应的热效应变大 | |
| C. | 相同温度下,起始时向容器中充入5molNO2和1.25molO2,达到平衡时,NO2的转化率小于50% | |
| D. | 达到平衡后,相同条件下往容器中充入2.5molN2O5和1.25molO2,此时平衡将向右移动 |
15.室温下,在强酸性和强碱性溶液中都不能大量共存的离子组是( )
| A. | NH${\;}_{4}^{+}$、Cu2+、Cl-、NO${\;}_{4}^{2-}$ | B. | K+、Na+、CO${\;}_{3}^{2-}$、S2- | ||
| C. | K+、Na+、CH3COO-、SO${\;}_{4}^{2-}$ | D. | Ba2+、Mg2+、HCO${\;}_{3}^{-}$、Cl- |
12.下列条件下,两瓶气体所含原子数一定相等的是( )
| A. | 同质量、不同密度的N2和CO2 | B. | 同温度、同体积的H2和N2 | ||
| C. | 同体积、同密度的O2和O3 | D. | 同压强、同体积的NO2和CO2 |
13.制取水煤气的反应为C(s)+H2O(g)═CO(g)+H2(g)△H>0,欲提高反应的速率和C(s)的转化率,可采用的措施为( )
| A. | 降温 | B. | 增大水蒸气的浓度 | ||
| C. | 增大C(s)的量 | D. | 增大压强 |