题目内容
【题目】下列离子方程式书写正确的是( )
A.向碳酸钠溶液中加入足量的盐酸:CO32-+2H+=CO2↑+H2O
B.氢氧化钡溶液中加入足量稀硫酸:Ba2++OH-+H++SO42-=BaSO4↓+H2O
C.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++H2O![]() Fe(OH)3↓+H+
Fe(OH)3↓+H+
D.澄清石灰水中加盐酸:Ca(OH)2 +2H+ = Ca2+ + 2H2O
【答案】A
【解析】
A. 向碳酸钠溶液中加入足量的盐酸生成二氧化碳和水:CO32-+2H+=CO2↑+H2O,故A正确;
B. 氢氧化钡溶液中加入足量稀硫酸生成硫酸钡和水:Ba2++2OH-+2H++SO42-=BaSO4↓+2H2O,故B错误;
C. 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O![]() Fe(OH)3(胶体)+3H+,故C错误;
Fe(OH)3(胶体)+3H+,故C错误;
D. 澄清石灰水中加盐酸: OH- +H+ = H2O,故D错误;
答案选A。

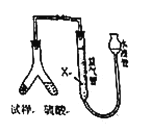
【题目】资料表明:赤热铜能与NO2反应。某小组设计了如下实验装置进行探究,探究固体产物的成分,气体产物是N2还是NO。
已知:酸性KMnO4溶液能氧化NO生成NO3ˉ;
NO和FeSO4溶液反应:NO+FeSO4=[Fe(NO)]SO4(棕色);
Cu2O+2H+=Cu+Cu2++H2O

请回答下列问题:
(1)A中反应的化学方程式为________________________。
(2)检查装置气密性,装好药品,然后实验的正确操作顺序是____________
①关闭K1,打开K2 ②打开分液漏斗活塞
③打开K1,关闭K2 ④点燃C处酒精灯
(3)实验过程中,D装置中的现象是____________,能否根据D装置中的现象确认C中有无NO生成? ______,理由是________________________。
(4)E装置的作用是____________。
(5)当铜粉完全反应后,实验小组对反应后的固体成分提出以下猜想:①只有CuO;②只有Cu2O;有同学认为可通过简单的定性实验即可判断猜想①是否成立,其实验方法是_____________________。
(6)实验中E装置自始至终未显棕色,小组最后通过定量实验得到如下数据。
C装置质量 | F装置气体的体积(已折算为标准状况) | ||
玻管质量 | Cu质量 | 反应后(玻管+生成物) | |
mg | 1.92g | (m+2.24)g | 112mL |
据此写出实验时实际发生反应的化学方程式________________________。