题目内容
【题目】为测定碳酸钠纯度(只含有少量氯化钠),学生设计了如下两个实验方案。
[方案1]称取![]() 样品,置于小烧杯中,加适量水完全溶解;向小烧杯中加入足量氢氧化钡溶液,过滤,洗涤、干燥沉淀,称量沉淀的质量为19.700克,计算。
样品,置于小烧杯中,加适量水完全溶解;向小烧杯中加入足量氢氧化钡溶液,过滤,洗涤、干燥沉淀,称量沉淀的质量为19.700克,计算。
(1)写出生成沉淀的反应方程式__________________。
(2)过滤操作需要的玻璃仪器__________________。
(3)计算碳酸钠的质量分数为______________(保留两位小数)。
[方案2]用下图装置,排液法测定![]() 的体积,并根据样品质量和
的体积,并根据样品质量和![]() 的体积计算
的体积计算
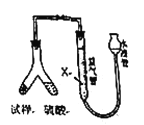
(4)为了减小测定![]() 的体积误差,量气管中加入的液体
的体积误差,量气管中加入的液体![]() 为______(填化学式)。
为______(填化学式)。
(5)通过实验,测得该试样中碳酸钠的质量分数偏高,产生这种现象的原因可能是______。
A.测定气体体积时未冷却至室温
B.气体进入量气管前未用浓硫酸干燥
C.![]() 型管中留有反应生成的气体
型管中留有反应生成的气体
D.反应结束后读数时水准管的水面高于量气管的水面
【答案】![]() 烧杯、玻璃棒、漏斗 0.88
烧杯、玻璃棒、漏斗 0.88 ![]() A
A
【解析】
(1)碳酸钠与氢氧化钡反应,生成碳酸钡和氢氧化钠,反应方程式为![]() ;
;
(2)过滤操作需要的玻璃仪器为烧杯、玻璃棒、漏斗。
(3)设样品中所含碳酸钠的质量为x
![]()
106g 197g
X 19.700g
由此求出x=10.600g
碳酸钠的质量分数为![]()
(4)为了减小测定![]() 的体积误差,即尽可能减少二氧化碳的溶解损失,量气管中加入的液体
的体积误差,即尽可能减少二氧化碳的溶解损失,量气管中加入的液体![]() 为饱和碳酸氢钠溶液。
为饱和碳酸氢钠溶液。
(5)A.测定气体体积时未冷却至室温,气体体积膨胀,排出的气体量多,量出的气体体积大,测得该试样中碳酸钠的质量分数偏高;
B.气体进入量气管前未用浓硫酸干燥,在排液时溶解在溶液中,不产生误差;
C.![]() 型管中留有反应生成的气体,气体替换了反应器内的空气,不产生误差;
型管中留有反应生成的气体,气体替换了反应器内的空气,不产生误差;
D.反应结束后读数时水准管的水面高于量气管的水面,读取的体积偏小,测得该试样中碳酸钠的质量分数偏低。
故选A。