题目内容
10.常温下,足量的铝,分别与下列酸反应时,放出H2最多的是( )| A. | 600mL 18.4mol/L H2SO4 | B. | 100mL 1mol/L HCl | ||
| C. | 200mL 80% HNO3 | D. | 600mL 0.1mol/L HNO3 |
分析 A、铝在冷的浓硫酸中发生钝化;
B、铝与盐酸反应生成氢气;
C、与与浓硝酸发生钝化现象,而与稀硝酸产生氮的氧化物;
D、与硝酸反应不产生氢气,而产生氮的氧化物.
解答 解:A、600mL 18.4mol/L H2SO4,铝在冷的浓硫酸中发生钝化,生成氢气为0;
B、100mL 1mol/L HCl,根据氢守恒,生成0.05mol的氢气;
C、200mL 80% HNO3,与浓硝酸发生钝化现象,不生成氢气;
D、与硝酸反应不产生氢气,而产生氮的氧化物;
综上所述,故选B.
点评 本题综合考查铁、硝酸、硫酸的性质,侧重于学生的分析能力和计算能力的考查,注意把握硝酸、浓硫酸与铝反应的特点,为易错点,难度不大.

练习册系列答案
相关题目
20.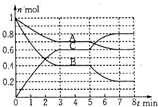 在一固定容积为2L的密闭容器中,气态物质A、B、C的物质量n(mol)随时间t(min)的变化如图所示.已知:平衡后,降低温度,A的转化率增大.下列选项中,能表明该反应一定达到平衡状态的是( )
在一固定容积为2L的密闭容器中,气态物质A、B、C的物质量n(mol)随时间t(min)的变化如图所示.已知:平衡后,降低温度,A的转化率增大.下列选项中,能表明该反应一定达到平衡状态的是( )
 在一固定容积为2L的密闭容器中,气态物质A、B、C的物质量n(mol)随时间t(min)的变化如图所示.已知:平衡后,降低温度,A的转化率增大.下列选项中,能表明该反应一定达到平衡状态的是( )
在一固定容积为2L的密闭容器中,气态物质A、B、C的物质量n(mol)随时间t(min)的变化如图所示.已知:平衡后,降低温度,A的转化率增大.下列选项中,能表明该反应一定达到平衡状态的是( )| A. | V正(A)=2V逆(B) | B. | 容器内混合气体的密度保持不变 | ||
| C. | 容器内的总压强保持恒定 | D. | A、B的转化率之比为1:2 |
18.在FeCl3溶液中,c(Fe3+)与c(Cl-)的关系是( )
| A. | c(Fe3+)=c(Cl-) | B. | 3c(Fe3+)=c(Cl-) | C. | 3c(Fe3+)>c(Cl-) | D. | 3c(Fe3+)<c(Cl-) |
5.常温下,1L pH=3的H2SO4溶液与下列溶液混合,其说法正确的是( )
| A. | 与等体积pH=11的氨水混合后所得溶液pH小于7 | |
| B. | 与pH=3的CH3COOH溶液混合后所得溶液pH小于3 | |
| C. | 与等浓度的CH3COONa溶液混合后所得溶液pH一定小于7 | |
| D. | 与10L Ba(OH)2溶液恰好完全反应,则Ba(OH)2溶液的pH一定等于10 |
15.不用其他化学试剂(可以加热或利用水)就能区别开的一组物质是( )
| A. | 苯、甲苯、四氯化碳 | B. | 酒精、硝基苯、四氯化碳 | ||
| C. | 溴苯、苯、四氯化碳 | D. | 酒精、甲苯、四氯化碳 |
6.下列分子中所有原子都满足最外层8电子结构的是( )
①SF6 ②PCl5 ③PCl3 ④CS2 ⑤NO2 ⑥N2.
①SF6 ②PCl5 ③PCl3 ④CS2 ⑤NO2 ⑥N2.
| A. | ①②④⑤ | B. | ②③⑤⑥ | C. | ③④⑥ | D. | ①③⑤ |
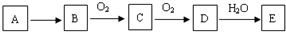
 ,A既能与强酸又能与强碱反应,且都能产生气体,则A的化学式为(NH4)2S或NH4HS.
,A既能与强酸又能与强碱反应,且都能产生气体,则A的化学式为(NH4)2S或NH4HS.