题目内容
20.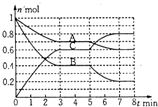 在一固定容积为2L的密闭容器中,气态物质A、B、C的物质量n(mol)随时间t(min)的变化如图所示.已知:平衡后,降低温度,A的转化率增大.下列选项中,能表明该反应一定达到平衡状态的是( )
在一固定容积为2L的密闭容器中,气态物质A、B、C的物质量n(mol)随时间t(min)的变化如图所示.已知:平衡后,降低温度,A的转化率增大.下列选项中,能表明该反应一定达到平衡状态的是( )| A. | V正(A)=2V逆(B) | B. | 容器内混合气体的密度保持不变 | ||
| C. | 容器内的总压强保持恒定 | D. | A、B的转化率之比为1:2 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:由图可知,A、B为反应物,C为生产物,且最后A、B的物质的量不为0,为可逆反应,3min时△n(A):△n(B):△n(C)=(1-0.7)mol:(1-0.4)mol:0.6mol=1:2:2,物质的量之比等于化学计量数之比,所以反应方程式为A+2B?2C,
A、V正(A)=$\frac{1}{2}$V正(B)=2V逆(B),故A错误;
B、容器中气体的密度始终不变,所以不能作平衡状态的标志,故B错误;
C、容器内的总压强保持恒定,说明气体的物质的量相等,达平衡状态,故C正确;
D、A、B起始投料量相等,而变化是1:2,所以转化率之比始终为1:2,故D错误;
故选C.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
相关题目
10.下列能用H++OH-=H2O表示的是( )
| A. | 稀硫酸和氢氧化钡溶液反应 | B. | 稀硝酸与氢氧化钠溶液反应 | ||
| C. | 醋酸与氢氧化钾溶液反应 | D. | 盐酸与氢氧化铁反应 |
11.化学与生产、生活密切相关.下列说法正确的是( )
| A. | 石英可导电,用于生产光导纤维 | |
| B. | 常见的氮肥都属于铵盐类无机物 | |
| C. | 粗盐经过溶解、过滤、蒸发结晶,即可得到纯净物氯化钠 | |
| D. | 生活中食用的食醋、植物油、动物蛋白等物质都是混合物 |
15.如表是周期表中的一部分,根据A-I在周期表中的位置,第(1)~(3)小题用元素符号或化学式回答,(4)~(6)小题按题目要求回答.
(1)最高价氧化物的水化物碱性最强的物质是Mg(OH)2,呈两性的物质是Al(OH)3.
(2)A分别与D、E、F、G、H形成的化合物中,最稳定的物质是HF
(3)在B、C、E、F、G、H中,原子半径最大的是Mg
(4)A和E组成的最简单化合物的结构式
(5)用电子式表示B和H组成化合物的形成过程
(6)H的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式6H++Al2O3=2Al3++3H2O.
| 族 周期 | I A | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | O |
| 1 | A | |||||||
| 2 | D | E | G | I | ||||
| 3 | B | C | F | H |
(2)A分别与D、E、F、G、H形成的化合物中,最稳定的物质是HF
(3)在B、C、E、F、G、H中,原子半径最大的是Mg
(4)A和E组成的最简单化合物的结构式

(5)用电子式表示B和H组成化合物的形成过程

(6)H的最高价氧化物的水化物和C的最高价氧化物相互反应的离子方程式6H++Al2O3=2Al3++3H2O.
5.下列各组物质熔化或气化时,所克服的微粒间的作用力属同种类型的是( )
| A. | SiO2和CaO的熔化 | B. | 氧化钠和铁的熔化 | ||
| C. | 碘和干冰的气化 | D. | 晶体硅和晶体硫的熔化 |
12.关于下列装置说法正确的是( )
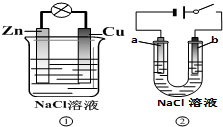

| A. | 装置①中的铜棒上冒气泡 | |
| B. | 若b是惰性电极,则装置②中的a、b 冒气泡 | |
| C. | 装置①换上硫酸铜溶液,将实现锌片上镀铜 | |
| D. | 装置②换上硫酸铜溶液,将实现“b极”镀铜 |
9.下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
| 物质 组别 | 甲 | 乙 | 丙 |
| A | SO2 | Ba(OH)2 | NaHCO3 |
| B | Na2O2 | H2O | CO2 |
| C | Na2SiO3 | NaOH | HCl |
| D | Al | H2SO4 | NaOH |
| A. | A | B. | B | C. | C | D. | D |
10.常温下,足量的铝,分别与下列酸反应时,放出H2最多的是( )
| A. | 600mL 18.4mol/L H2SO4 | B. | 100mL 1mol/L HCl | ||
| C. | 200mL 80% HNO3 | D. | 600mL 0.1mol/L HNO3 |
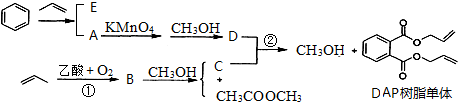

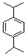 .
. .
.