��Ŀ����
����Ŀ�����ܱ������з�����Ӧ2SO2(g)+O2(g) 2SO3(g) ��H<0��ij�о�С���о���������������ʱ���ı�ijһ������������Ӧ��Ӱ�죬���ͼ�����з�����ȷ����
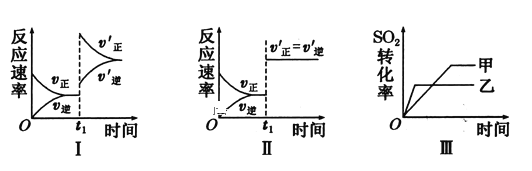
A.ͼI�о�����t1ʱ�������¶ȶԷ�Ӧ���ʵ�Ӱ��
B.ͼI�о����Ǽ�����ʴ����Է�Ӧ���ʵ�Ӱ��
C.ͼII�о�����t1ʱ��ͨ�뺤�������ֺ��ݣ��Է�Ӧ���ʵ�Ӱ��
D.ͼIII�о������¶ȶԻ�ѧƽ���Ӱ�죬���ҵ��¶Ƚϸ�
���𰸡�D
��������
A�������¶ȣ����淴Ӧ���ʾ�˲���������ȷ����淴Ӧ��������Ķ�Щ�����ı�����˲��v����v����ƽ�������ƶ�����ͼ����v����v������A����
B��������ʴ�����ͬ�ȳ̶ȸı䷴Ӧ���ʣ���ƽ�ⲻ�ƶ�����B����
C��ͨ�뺤��(���ֺ���)����Ӧ���ʲ��䣬ƽ�ⲻ�ƶ���ͼ��t1ʱ�̲���ͨ�뺤��(���ֺ���)�Է�Ӧ���ʵ�Ӱ�죬��C����
D���÷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ�������ƶ�����Ӧ���ʼӿ죬���������ת���ʼ�С��ͼ���ҵ�ʱ���٣���ͼ���о������¶ȶԻ�ѧƽ���Ӱ�죬���ҵ��¶Ƚϸߣ���D��ȷ��
�ʴ�ΪD��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��ij��ѧС��Ϊ���о���������Ի�ѧ��Ӧ���ʵ�Ӱ�죬���������Ը�����������ķ�Ӧ����¼����ʵ�����ݣ�
ʵ���� | ʵ���¶� | �Թ��������Լ��������� / mL | ��Һ������ɫ����ʱ��/ min | |||
0.6mol/L H2C2O4 ��Һ | H2O | 3mol/L H2SO4 ϡ��Һ | 0.05mol/L KMnO4��Һ | |||
�� | 25 | 3.0 | V1 | 2.0 | 3.0 | 1.5 |
�� | 25 | 2.0 | 3.0 | 2.0 | 3.0 | 2.7 |
�� | 50 | 2.0 | V2 | 2.0 | 3.0 | 1.0 |
��1����д���÷�Ӧ�����ӷ���ʽ__________________________________________,���÷�Ӧ�Ա������ݷ�Ӧ��ȫʱת�Ƶ�����Ϊ_______________NA
��2��V1 ______
��3�������ϱ��е�ʵ����������������Եõ��Ľ�����_____��
��4��̽���¶ȶԻ�ѧ��Ӧ���ʵ�Ӱ����Ӧѡ��_____����ʵ���ţ�
��5����С��ͬѧ���ݾ�������� n ��Mn 2+ ����ʱ��仯��������ͼ 1 ��ʾ������ͬѧ�������е�ʵ�����Ϸ�������ʵ������� n ��Mn 2+ �� ��ʱ��仯��ʵ��������ͼ 2 ��ʾ��
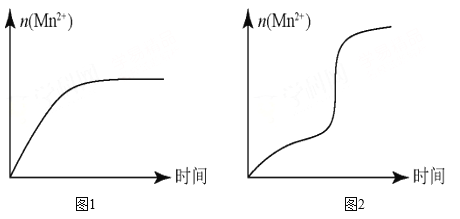
��С��ͬѧ����ͼ 2 ��ʾ��Ϣ������µļ��������������ʵ�鷽����������ʵ��̽����
ʵ���� | ʵ���¶�/�� | �Թ��������Լ��������� | �ټ���ij�ֹ��� | ��Һ������ɫ����ʱ�� / min | |||
�� | 25 | 0.6mol/L H2C2O4 ��Һ | H2O | 3mol/L H2SO4 ϡ��Һ | 0.05mol/L KMnO4 ��Һ | ||
2.0 | 3.0 | 2.0 | 3.0 | MnSO4 | t | ||
�ٸ�С��ͬѧ����ļ�����_____��
������С��ͬѧ����ļ��������Ӧ�۲쵽_________________________________����