题目内容
17.影响水的电离平衡的因素,观察下表的数据:| t(℃) | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
| Kw/10-14 | 0.134 | 0.292 | 0.681 | 1.01 | 2.92 | 5.47 | 38.0 | 55.0 |
(2)以上数据说明温度与水的电离程度之间存在什么关系?
[小结]:在H2O?H++OH-:
升高温度,水的电离程度增大,水的电离平衡向正向移动,KW增大.
降低温度,水的电离程度减小,水的电离平衡向逆向移动,KW减小.
分析 (1)由题干所给数据找出水的KW与温度的关系、判断水的电离平衡的移动方向,通过移动方向判断水的电离是吸热还是放热;
(2)纯水中加入盐酸,增大了c(H+),使溶液呈酸性,纯水中加氢氧化钠,增大了c(OH-),溶液呈碱性;根据影响化学反应平衡的因素和KW只受温度的影响分析.
解答 解:(1)由题干所给数据可知水的KW与温度成正比,即随着温度的升高,KW的值增大,由Kw=c(H+)•c(OH-)可知,c(H+)和c(OH-)增大,水的电离程度增大,水的电离平衡向右移动,说明水的电离是吸热的过程,
故答案为:随着温度的升高,KW的值增大,c(H+)和c(OH-)增大,水的电离程度增大,水的电离平衡向右移动,说明水的电离是吸热的过程;
(2)由表中所给数据可知:水的电离是吸热的过程,温度升高促进水的电离,电离平衡正向进行,氢离子、氢氧根离子浓度增大,Kw增大,降低温度,水的电离程度减小,电离平衡逆向进行,Kw减小,
故答案为:增大,正向,增大.减小,逆向,减小.
点评 本题考查了水的电离、离子积常数,题目难度不大,注意水的离子积常数只受温度的影响.

练习册系列答案
相关题目
8.分类是科学研究的重要方法,下列物质分类不正确的是( )
| A. | 化合物:干冰,冰水混合物,烧碱,小苏打 | |
| B. | 同素异形体:活性炭,C60,C80,金刚石 | |
| C. | 非电解质:乙醇,四氯化碳,氯气,葡萄糖 | |
| D. | 混合物:漂白粉,纯净矿泉水,盐酸,石灰石 |
5.下列说法错误的是( )
| A. | 金属钠着火可用干燥沙土扑灭 | |
| B. | 地沟油经处理后可用作生物柴油 | |
| C. | 糖类、油脂、蛋白质均为高分子化合物 | |
| D. | 氢氧化铁胶体的分散质粒子能通过滤纸孔隙 |
12.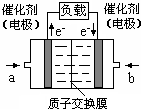 可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.下列说法不正确的是( )
可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.下列说法不正确的是( )
 可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.下列说法不正确的是( )
可给笔记本电脑供电的甲醇燃料电池已经面世,其结构示意图如下.甲醇在催化剂作用下提供质子(H+)和电子,电子经外电路、质子经内电路到达另一电极后与氧气反应,电池总反应为:2CH3OH+3O2=2CO2+4H2O.下列说法不正确的是( )| A. | 右电极为电池正极,b处通入的物质是空气 | |
| B. | 左电极为电池负极,a处通入的物质是空气 | |
| C. | 负极反应式为:CH3OH+H2O-6e-=CO2+6H+ | |
| D. | 正极反应式为:O2+4H++4e-=2H2O |
2.下列离子方程式书写正确的是( )
| A. | 等体积等物质的量浓度的氢氧化钡溶液与碳酸氢铵溶液混合:Ba2++2OH-+NH4++HCO3-=BaCO3↓+NH3•H2O+H2O | |
| B. | 氯化铝溶液中加入过量的氨水:Al3++4 NH3•H2O=4NH4++AlO2-+2H2O | |
| C. | 向次氯酸钙溶液中通入少量的二氧化硫:Ca2++2ClO-+SO2+H2O=CaSO3↓+2HClO | |
| D. | 碳酸钠溶液中加入过量的苯酚: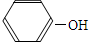 +CO32-= +CO32-= +HCO3- +HCO3- |
9.下列有关胶体和溶液的比较中,正确的是( )
| A. | 溶液中溶质粒子不带电,胶体分散质粒子带电 | |
| B. | 溶液中溶质的粒子运动有规律,胶体粒子运动无规律 | |
| C. | 通直流电后,溶液中溶质的粒子分别向两极运动,而胶体中分散质的粒子向某一极运动 | |
| D. | 溶液中通过一束光线没有特殊现象,胶体中通过一束光线出现光亮的“通路” |
6.根据下列反应判断有关物质还原性由强到弱的顺序是( )
H2SO3+I2+H2O═2HI+H2SO4 2FeCl3+2HI═2FeCl2+2HCl+I2
3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
H2SO3+I2+H2O═2HI+H2SO4 2FeCl3+2HI═2FeCl2+2HCl+I2
3FeCl2+4HNO3═2FeCl3+NO↑+2H2O+Fe(NO3)3.
| A. | NO>FeCl2>H2SO3>HI | B. | HI>FeCl2>H2SO3>NO | ||
| C. | FeCl2>HI>H2SO3>NO | D. | H2SO3>HI>FeCl2>NO |
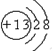 ,由A和B形成的含有非极性键的离子化合物的电子式是
,由A和B形成的含有非极性键的离子化合物的电子式是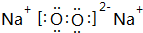 ;
;