题目内容
6.短周期元素X、Y、Z的原子序数依次递增,它们的原子最外层电子数之和为11,X、Z同主族,Y原子最外层电子数比X原子次外层电子数多1.下列叙述正确的是( )| A. | Y的最高价氧化物的熔点比X的最高价氧化物的熔点低 | |
| B. | 原子半径:Y>Z>X | |
| C. | Y的最高价氧化物的水化物只能与酸反应,不能与碱反应 | |
| D. | 由Z、Y两元素分别形成的单质均存在同素异形体 |
分析 短周期元素X、Y、Z的原子序数依次递增,X、Z同主族,则X处于第二周期、Y处于第三周期,Y原子最外层电子数比X原子次外层电子数多1,则Y原子最外层电子数为3,它们的原子最外层电子数之和为11,则X、Z原子最外层电子数为$\frac{11-3}{2}$=4,可推知X为C元素、Z为Si、Y为Al,据此解答.
解答 解:短周期元素X、Y、Z的原子序数依次递增,X、Z同主族,则X处于第二周期、Y处于第三周期,Y原子最外层电子数比X原子次外层电子数多1,则Y原子最外层电子数为3,它们的原子最外层电子数之和为11,则X、Z原子最外层电子数为$\frac{11-3}{2}$=4,可推知X为C元素、Z为Si、Y为Al.
A.氧化铝属于离子晶体,二氧化碳属于分子晶体,常温下为气体,故氧化铝的熔点高于二氧化碳的熔点,故A错误;
B.同周期自左而右原子半径减小、同主族自上而下原子半径增大,故原子半径Y(Al)>Z(Si)>X(C),故B正确;
C.Y的最高价氧化物的水化物为氢氧化铝,属于两性氢氧化物,能与酸、碱反应,故C错误;
D.硅单质存在晶体硅与无定形硅,而铝单质不存在同素异形体,故D错误,
故选B.
点评 本题考查结构性质位置关系综合应用,推断元素是解题关键,注意微粒半径比较与元素化合物性质的掌握.

练习册系列答案
相关题目
16.烷烃C5H12的同分异构体数目是( )
| A. | 2 | B. | 3 | C. | 4 | D. | 5 |
17.如图是恒温下某反应的化学反应速率随反应时间变化的示意图.下列叙述与示意图不相符合的是( )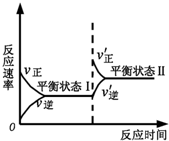

| A. | 反应达平衡时,正反应速率和逆反应速率相等 | |
| B. | 该反应达到平衡状态Ⅰ后,减小反应物浓度,平衡发生移动,达到平衡状态Ⅱ | |
| C. | 该反应达到平衡状态Ⅰ后,增大反应物浓度,平衡发生移动,达到平衡状态Ⅱ | |
| D. | 同一种反应物在平衡状态Ⅰ和平衡状态Ⅱ时浓度不相等 |
14.NA为阿伏伽德罗常数的值.下列叙述正确的是( )
| A. | 常温下,2LpH=12的氨水中含有OH-数目为0.02NA | |
| B. | 氯碱工业中,外电路中转移电子数为0.3NA时产生气体体积(标准状况)为4.48L | |
| C. | 标准状况下,11.2LCH3Cl中非极性共价键数目等于2.0NA | |
| D. | 一定条件下,1molI2和0.2molH2混合充分反应,转移的电子数为0.4NA |
1.磷矿石主要以碳酸钙[Ca3(PO4)2•H2O]和磷灰石[Ca5F(PO4)3]等形式存在.目前国际上磷矿石利用大致有湿法磷酸和热法磷酸两种工艺.其中湿法磷酸是指磷酸矿石用过量硫酸分解制备磷酸.热法磷酸指用过量焦炭、二氧化硅与磷灰石在高温下获得单质磷,然后再由磷制备磷酸.
部分物质的相关性质如下:
(1)以磷矿石为原料,湿法磷酸过程中Ca5F(PO4)3反应的化学方程式为Ca5F(PO4)3+5H2SO4=3H3PO4+5CaSO4+HF↑.现有1吨折合含有五氧化二磷约30%的磷灰石,最多可制得到70%的商品磷酸0.59吨.
(2)热法生产磷酸反应过程中产生大量炉渣和尾气,其中炉渣的主要成分是:CaSiO3(填化学式).尾气中主要含有SiF4、CO(均填化学式).还含有少量PH3、H2S和HF等.将其通入纯碱溶液中可除去气体SiF4、H2S和HF,再通入NaClO溶液可除去具有还原性的PH3气体,写出该反应的离子方程式2PH3+3ClO-=2P+3Cl-+3H2O.
部分物质的相关性质如下:
| 熔点/℃ | 沸点/℃ | 备注 | |
| 白磷 | 44 | 280.5 | |
| PH3 | -133.8 | -87.8 | 难溶于水、有还原性 |
| SiF4 | -90 | -86 | 易水解 |
(2)热法生产磷酸反应过程中产生大量炉渣和尾气,其中炉渣的主要成分是:CaSiO3(填化学式).尾气中主要含有SiF4、CO(均填化学式).还含有少量PH3、H2S和HF等.将其通入纯碱溶液中可除去气体SiF4、H2S和HF,再通入NaClO溶液可除去具有还原性的PH3气体,写出该反应的离子方程式2PH3+3ClO-=2P+3Cl-+3H2O.
11.a、b、c、d四个金属电极,有关的实验装置现象如表所示:由此判断这四个电极对应的金属活动性由强到弱的顺序为
( )
( )
| 装置 | 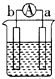 CuSO4溶液 | 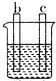 稀硫酸 |  稀硫酸 |
| 现象 | a极质量减小 b极质量增大 | b极有气泡 c极无明显现象 | 电流从a极流向d极 |
| A. | d>a>b>c | B. | b>c>d>a | C. | a>b>c>d | D. | a>b>d>c |
18.用铝热法还原下列化合物,当各制得1mol金属单质时,消耗铝的质量最少的是( )
| A. | CO3O4 | B. | WO3 | C. | MnO2 | D. | Cr2O3 |
16.用NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A. | 一定条件下,将1molN2和3molH2混合,充分反应后转移的电子数为NA | |
| B. | 1.5molNO2与足量水反应,转移的电子数为1.5NA | |
| C. | 6.4g由S2、S4、S8组成的混合物含硫原子数为0.2NA | |
| D. | 常温常压下,11.2LCl2含氯原子数为NA |

 ;
;