题目内容
7.下列原子序数所对应的元素组中,两者可形成离子键的是( )| A. | 1和17 | B. | 15和8 | C. | 14和 6 | D. | 12和9 |
分析 活泼金属和活泼非金属元素之间易形成离子键,同种非金属元素之间形成非极性共价键,不同非金属元素之间形成极性共价键,据此分析解答.
解答 解:A.1号元素是H元素、17号元素是Cl元素,二者只能形成非极性键共价键,故A错误;
B.15、8号元素分别是P、O元素,二者都是较活泼非金属元素,只能形成极性键,故B错误;
C.14、6号元素分别是Si、C元素,二者都是非金属元素,只能形成极性键,故C错误;
D.12、9号元素分别是Mg、F元素,二者通过得失电子形成离子键,故D正确;
故选D.
点评 本题考查化学键判断,侧重考查基本概念,明确离子键、共价键的区别是解本题关键,注意常见物质的结构及其构成微粒,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
17.某无色溶液能与铁粉反应放出大量氢气,此溶液中可能大量共存的离子组是( )
| A. | H+、K+、Mg2+、Cl- | B. | Ba2+、SO42-、Cl-、OH- | ||
| C. | K+、OH-、CO32-、MnO4- | D. | Ca2+、H+、Cl-、HCO3- |
18.已知热化学方程式:C2H2(g)+$\frac{5}{2}$O2(g)═2CO2(g)+H2O(g)△H=-1256kJ•mol-1.下列说法正确的是( )
| A. | C2H2的燃烧热为1256kJ/mol | |
| B. | 若生成2mol液态水,则△H=-2512kJ/mol | |
| C. | 若转移10mol电子,则消耗2.5mol O2 | |
| D. | 若形成4mol碳氧共用电子对,则放出的热量为2512kJ |
2.下列有机物中,完全燃烧时生成的二氧化碳与水的物质的量之比为2:1的是( )
| A. | 乙烷 | B. | 乙烯 | C. | 乙炔 | D. | 乙醇 |
12.关于下列各图的叙述中,正确的是( )
| A. | 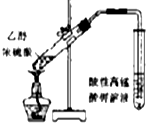 如图装置检验加热时产生的乙烯 | |
| B. | 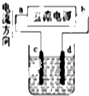 如图装置精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液. | |
| C. | 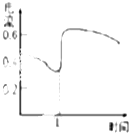 如图表示Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2 | |
| D. | 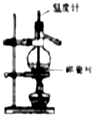 如图装置分离溴的四氯化碳溶液 |
19.在下列各溶液中,一定能大量共存的一组离子是( )
| A. | 含有AlO2-的溶液中:Na+、Al3+、NO3-、Cl- | |
| B. | 使淀粉碘化钾变蓝的溶液中:K+、HCO3-、S2-、SO42- | |
| C. | 能与金属铝反应放出氢气的溶液中:K+、NO3-、Cl-、Na+ | |
| D. | 透明溶液中:Na+、MnO4-、Na+、SO42- |
16.将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72 L,若反应过程中溶液的体积保持不变,则下列说法正确的是( )
| A. | 标准状况下,反应过程中得到7.84 L的气体 | |
| B. | 最终得到的溶液中c(Na+)=c(Cl-)+c(OH-) | |
| C. | 最终得到7.8 g的沉淀 | |
| D. | 最终得到的溶液中c(Na+)=1.5 mol•L-1 |
 现有一盛有无色固体物质M的试剂瓶,标签已破损(见图).
现有一盛有无色固体物质M的试剂瓶,标签已破损(见图). 向100mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),测得最后溶液的pH>7.
向100mL NaOH溶液中逐渐通入一定量的CO2(假设溶液体积不变),测得最后溶液的pH>7.