题目内容
17.某无色溶液能与铁粉反应放出大量氢气,此溶液中可能大量共存的离子组是( )| A. | H+、K+、Mg2+、Cl- | B. | Ba2+、SO42-、Cl-、OH- | ||
| C. | K+、OH-、CO32-、MnO4- | D. | Ca2+、H+、Cl-、HCO3- |
分析 无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,与铁粉反应放出大量氢气的溶液中存在大量氢离子,
A.四种离子之间不反应,都是无色离子,加入铁粉能够放出氢气;
B.钡离子与硫酸根离子反应生成硫酸钡沉淀,氢氧根离子与氢离子反应;
C.高锰酸根离子为有色离子,不满足溶液无色的条件;
D.氢离子与碳酸氢根离子反应生成二氧化碳气体.
解答 解:无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,与铁粉反应放出大量氢气的溶液中存在大量氢离子,
A.H+、K+、Mg2+、Cl-之间不发生反应,都是无色离子,加入铁粉后能够产生大量氢气,故A正确;
B.Ba2+、SO42-之间反应生成难溶物硫酸钡,在溶液中不能大量共存,故B错误;
C.MnO4-为有色离子,不满足溶液无色的要求,故C错误;
D.H+、HCO3-之间发生反应生成二元化气体和水,在溶液中不能大量共存,故D错误;
故选A.
点评 本题考查离子共存的判断,题目难度中等,注意掌握离子反应发生条件,明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生络合反应的离子之间(如 Fe3+和 SCN-)等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
相关题目
14.有机物分子中原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列事实不能说明上述观点的是( )
| A. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| B. | 发生硝化反应时,苯需要加热,甲苯在常温下就能进行 | |
| C. | 苯酚能跟NaOH溶液反应,乙醇不能与NaOH溶液反应 | |
| D. | 乙烯能发生加成反应,乙烷不能发生加成反应 |
5.下列离子方程式正确的是( )
| A. | 稀硫酸加入氢氧化钡溶液中:H++OH-═H2O | |
| B. | 铜片上滴加稀硝酸:3Cu+8H++2 NO3-═3Cu2++2NO↑+4H2O | |
| C. | 石灰石投入到稀醋酸中:CO32-+2 H+═CO2↑+H2O | |
| D. | Fe粉加入稀盐酸中:Fe+2H+═Fe2++H2↑ |
2.检验SO2中是否混有CO2气体,可采用的方法是( )
| A. | 通过品红溶液,若品红溶液褪色,则说明混有CO2气体 | |
| B. | 通过澄清石灰水,若变混浊,则说明混有CO2气体 | |
| C. | 先通过足量NaOH溶液,再通过澄清石灰水,若变混浊,则说明混有CO2气体 | |
| D. | 先通过足量KMnO4溶液(具有强氧化性),再通过澄清石灰水,若变混浊,则说明混有CO2气体 |
9.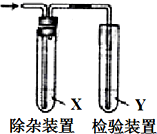 用如图所示装置检验气体时试剂X没必要或是错误的是( )
用如图所示装置检验气体时试剂X没必要或是错误的是( )
 用如图所示装置检验气体时试剂X没必要或是错误的是( )
用如图所示装置检验气体时试剂X没必要或是错误的是( )| 检验的气体 | 试剂X | 试剂Y | |
| A | CH3CH2Br与NaOH乙醇溶液共热制备的乙烯 | H2O | Br2的CCl4溶液 |
| B | CH3CH2OH与浓H2SO4共热170℃制备的乙烯 | NaOH溶液 | 酸性KMnO4溶液 |
| C | 电石与饱和食盐水反应制备的乙烯 | 水 | 酸性KMnO4溶液 |
| D | 苯,液溴,铁屑混合反应生成的HBr | CCl4 | 硝酸银溶液 |
| A. | A | B. | B | C. | C | D. | D |
6.下列物质在常温常压下呈气态的是( )
| A. | 甲醛 | B. | 甲酸 | C. | 甲醇 | D. | 甲苯 |
7.下列原子序数所对应的元素组中,两者可形成离子键的是( )
| A. | 1和17 | B. | 15和8 | C. | 14和 6 | D. | 12和9 |
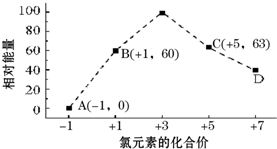 元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.
元素周期表中第ⅦA族元素的单质及其化合物的用途广泛.