题目内容
1.元素性质呈周期性变化的决定因素是( )| A. | 元素原子核外电子层排布呈周期性变化 | |
| B. | 元素相对原子质量依次递增 | |
| C. | 元素原子半径大小呈周期性变化 | |
| D. | 元素的最高正化合价呈周期性变化 |
分析 元素的性质由最外层电子决定,在周期表中的原子的电子层排布呈现周期性的变化,则元素的性质呈周期性的变化.
解答 解:A、元素的性质由最外层电子决定,随原子序数的递增,电子层数和最外层电子数都呈现周期性的变化而引起元素性质的周期性变化,即原子的电子层排布的周期性变化是引起元素性质周期性变化的决定因素,故A正确;
B、元素的原子的相对原子质量增大,但不呈现周期性的变化,则不能决定元素性质出现周期性变化,故B错误;
C、原子半径属于元素的性质,元素的原子半径的周期性变化是原子的电子排布周期性变化的结果,故C错误;
D、元素的最高正化合价的周期性变化是原子的电子排布周期性变化的结果,化合价属于元素的性质,故D错误;
故选:A.
点评 本题考查元素周期律,学生明确原子的电子排布是解答本题的关键,并应熟悉元素的性质来解答,题目难度不大.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案
相关题目
12.能用浓硫酸干燥的气体是( )
| A. | HI | B. | NH3 | C. | SO2 | D. | H2S |
9.某芳香烃的分子式为C10H14,不能使溴水褪色,分子结构中只含有一个侧链烃基,则此侧链烃基的结构共有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
6.下列物质属于同素异形体的是( )
| A. | 氕和氘 | B. | CH3CH3和CH3CH2CH3 | ||
| C. | 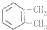 和 和 | D. | O2和O3 |
13.如表除去括号内杂质所用的试剂和方法都正确的是( )
| 选项 | 物质 | 所用试剂 | 方法 |
| A | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| B | 乙醇(水) | 生石灰 | 分液 |
| C | 乙醇(乙酸) | 氢氧化钠溶液 | 分液 |
| D | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 分液 |
| A. | A | B. | B | C. | C | D. | D |
10.用惰性电极电解下列溶液,电解一段时间后,阴极质量增加,电解液的pH下降的是( )
| A. | CuSO4 | B. | NaOH | C. | BaCl2 | D. | H2SO4 |
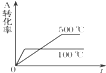
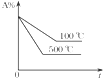
11.在容积不变的密闭容器中存在如下反应:2A(g)+B(g)?3C(g);△H<0,某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析正确的是( )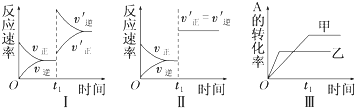

| A. | 图Ⅰ表示的是t1时刻增大反应物的浓度对反应速率的影响 | |
| B. | 图Ⅱ表示的一定是t1时刻加入催化剂后对反应速率的影响 | |
| C. | 图Ⅲ表示的是温度对化学平衡的影响,且乙的温度较高 | |
| D. | 图Ⅲ表示的是不同催化剂对平衡的影响,且甲的催化效率比乙高 |
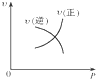
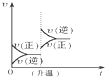
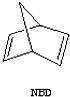
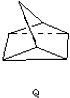 △H=+88.62kJ/mol
△H=+88.62kJ/mol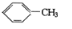 .若用氯原子取代NBD分子中的一个H原子,可得到的同分异构体共有3种.
.若用氯原子取代NBD分子中的一个H原子,可得到的同分异构体共有3种.