题目内容
(4分)(1)写出下列物质的化学式:①漂白粉的有效成分: ;②钡餐: 。
(2)写出用Na2SO3与浓H2SO4反应制备SO2的化学方程式: 。
(1)①Ca(ClO)2 ②BaSO4 (2)Na2SO3+H2SO4 Na2SO4+SO2+H2O
Na2SO4+SO2+H2O
解析试题分析:(1)①漂白粉的有效成分为Ca(ClO)2;②钡餐为BaSO4。(2)Na2SO3与浓H2SO4反应生成硫酸钠、水和SO2,化学方程式为Na2SO3+H2SO4 Na2SO4+SO2+H2O。
Na2SO4+SO2+H2O。
考点:考查元素化合物知识。

练习册系列答案
相关题目
有科学家预测,氨能有望取代氢能,成为重要的新一代绿色能源。下列有关说法不正确的是( )
| A.液氨作为清洁能源的反应原理是4NH3+5O2=4NO+6H2O |
| B.液氨具有腐蚀性和毒性,在使用过程中要防止氨泄漏 |
| C.氨气比空气轻,标准状况下密度约为0.76g·L-1 |
| D.氨与氢气相比,优点在于氨不容易发生爆炸,使用时更安全 |


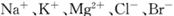 等离子)可提取溴,其生产流程如下:
等离子)可提取溴,其生产流程如下:


