题目内容
1. (1)已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.若向三份等体积、等物质的量浓度的NaOH溶液中分别加入醋酸、浓硫酸、稀硝酸至恰好完全反应,并将上述过程中放出的热量分别记为Q1kJ、Q2kJ、Q3kJ.则三者的由小到大关系是Q1<Q3<Q2(用Q1、Q2、Q3表示).
(1)已知H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1.若向三份等体积、等物质的量浓度的NaOH溶液中分别加入醋酸、浓硫酸、稀硝酸至恰好完全反应,并将上述过程中放出的热量分别记为Q1kJ、Q2kJ、Q3kJ.则三者的由小到大关系是Q1<Q3<Q2(用Q1、Q2、Q3表示).(2)如图所示A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,两个小孔不能开得过大,其目的是减少热量散失; 若实验中不加盖泡沫塑料板,则求得的中和热数值偏小(填偏大、偏小、无影响)
(3)实验室用50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1NaOH溶液利用如图装置,进行测定中和热的实验.假设盐酸和氢氧化钠溶液的密度都是1g/cm3,又知中和后生成溶液的比热容c=4.18J/(g•℃).为了计算中和热,实验时还需测量的数据有(填序号)ACE.
A.反应前盐酸的温度 B.反应前盐酸的质量
C.反应前氢氧化钠溶液的温度 D.反应前氢氧化钠溶液的质量
E.反应后混合溶液的最高温度 F.反应后混合溶液的质量
(4)某学生实验记录数据如下:
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 20.0 | 20.1 | 23.4 |
| 2 | 20.2 | 20.4 | 23.6 |
| 3 | 20.5 | 20.6 | 23.8 |
分析 (1)在稀溶液中,稀的强酸跟强碱发生中和反应而生成1mo水,这时的反应热叫做中和热.浓硫酸稀释是一个放热的过程,醋酸是弱电解质,电离时吸收热量,据此解答;
(2)根据测定中和热过程中必须尽量减少热量的散失分析;不盖硬纸板,会有一部分热量散失;
(3)根据中和热计算公式Q=cm△T中涉及的未知数据进行判断;
(4)先根据表中测定数据计算出混合液反应前后的平均温度差,再根据Q=cm△T计算出反应放出的热量,最后计算出中和热.
解答 解:(1)中和热是指在稀溶液中,稀的强酸跟强碱发生中和反应而生成1mo水放出的热量,但浓硫酸稀释也会放热,醋酸是弱电解质电离时吸收一部分热量,所以放出的总热量:Q1<Q3<Q2;
故答案为:Q1<Q3<Q2;
(2)如图所示,A为泡沫塑料板,上面有两个小孔,分别插入温度计和环形玻璃搅拌棒,若两个小孔开得过大,会导致散失较多的热量,影响测定结果;大烧杯上如不盖硬纸板,会有一部分热量散失,求得的中和热数值将会减小;
故答案为:减少热量散失;偏小;
(3)由Q=cm△T可知,测定中和热需要测定的数据为:反应前盐酸和氢氧化钠溶液的温度,反应前盐酸和氢氧化钠溶液的质量,反应后混合溶液的最高温度;
故选:ACE;
(4)第1次实验盐酸和NaOH溶液起始平均温度为20.05℃,反应后温度为23.4℃,反应前后温度差为3.35℃;
第2次实验盐酸和NaOH溶液起始平均温度为20.3℃,反应后温度为23.6℃,反应前后温度差为:3.3℃;
第3次实验盐酸和NaOH溶液起始平均温度为20.55℃,反应后温度为23.8℃,反应前后温度差为:3.25℃;
平均温度差为:3.3℃,50mL 0.50mol•L-1盐酸、50mL 0.55mol•L-1NaOH溶液的质量和为m=100mL×1g/cm3=100g,c=4.18J/(g•℃),代入公式Q=cm△T得生成0.025mol的水放出热量Q=4.18J/(g•℃)×100g×3.3℃=1.3794kJ,即生成1mol的水放出热量为=$\frac{1.3794kJ}{0.025}$kJ=55.2,即该实验测得的中和热△H=-55.2kJ/mol,
故答案为:-55.2kJ/mol.
点评 本题考查热化学方程式以及反应热的计算,题目难度大,注意理解中和热测定原理以及测定反应热的误差等问题,试题有利于培养学生灵活应用所学知识的能力.

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案| A. | 氧化铝陶瓷具有两性,可用来制造人造牙齿 | |
| B. | 氮化硅陶瓷耐高温且不易传热,可用来制造柴油机 | |
| C. | 光导纤维传导光的性能很强,是非常好的通讯材料 | |
| D. | 人造刚玉硬度高,用于制造刚玉球磨机 |
| 编号 | Ⅰ | Ⅱ | Ⅲ |
| 实验 |  |  | 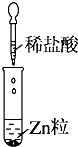 |
| 现象 | 没有明显变化,溶液仍为无色 | 有沉淀生成,溶液为蓝色 | 有无色气体放出 |
| A. | Ⅰ中无明显变化,说明两溶液不反应 | |
| B. | Ⅱ中的白色沉淀为BaSO4 | |
| C. | Ⅲ中的离子方程式为2H++Zn═Zn2++H2↑ | |
| D. | Ⅲ中发生的反应也是氧化还原反应 |
| A. | 碳酸钙溶于醋酸溶液中:CaCO3+2H+═Ca2++CO2↑+H2O | |
| B. | 氯化镁溶液和氨水混合:Mg2++2OH-═Mg(OH)2 | |
| C. | 铁与稀硝酸反应:Fe+2H+═Fe2++H2↑ | |
| D. | 铝片插入硝酸银溶液中 Al+3Ag+═Al3++3Ag |
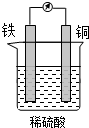
| A. | 铁片质量减小 | B. | 铜片质量不变 | ||
| C. | 铜片表面产生气泡 | D. | 溶液逐渐变蓝 |
| 化学式 | CH3COOH | H2CO3 | HClO | H2C4H4O6(酒石酸) | H2SO3 |
| 电离平衡常数 | 2.0×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 | K1=9.1×10-4 K2=4.3×10-5 | K1=1.3×10-2 K2=6.3×10-8 |
(1)pH相同的下列物质的溶液:a.Na2CO3,b.NaClO,c.CH3COONa d.NaHCO3 e.Na2C4H4O6;物质的量浓度由大到小的顺序是e c d b a(填字母).
(2)常温下,0.1mol/L的CH3COOH溶液的pH═2.85(已知lg2=0.3).
(3)常温下,将0.1mol/L的次氯酸溶液与0.1mol/L的碳酸钠溶液等体积混合,所得溶液中各种离子浓度关系正确的是BCE
A.c(Na+)>c(ClO-)>c(HCO3-)>c(OH-)
B.c(Na+)>c(HCO3-)>c(ClO-)>c(H+)
C.c(Na+)═c(HClO)+c(ClO-)+c(HCO3-)+c(H2CO3)+c(CO32-)
D.c(Na+)+c(H+)═c(ClO-)+c(HCO3-)+2c(CO32-)
E.c(HClO)+c(H+)+c(H2CO3)═c(OH-)+c(CO32-)
(4)写出少量的CO2通入NaClO溶液中的化学方程式CO2+NaClO+H2O=NaHCO3+HClO.
(5)0.1mol/L的酒石酸溶液与pH=13的NaOH溶液等体积混合,所得溶液的pH为6,则c(HC4H4O6-)+2c(C4H4O62-)=(0.05+10-6-10-8)mol/L.(用准确的数值表示)
| A. | 硝酸应保存在棕色试剂瓶里 | |
| B. | 铵态氮肥不宜与碱性肥料混合施用 | |
| C. | 往硝酸亚铁溶液中加稀硫酸无明显现象 | |
| D. | NO可用排水法收集,NO2可用向上排空气法收集 |
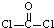 ,分子构型为平面三角形
,分子构型为平面三角形