题目内容
【题目】常温下用过量铁片与稀硫酸反应制取氢气,采取下列措施:
①不用铁片,改用铁粉;②加入少量![]() 溶液;③加入少量
溶液;③加入少量![]() 固体;④将稀硫酸换为
固体;④将稀硫酸换为![]() 的硫酸;⑤加入
的硫酸;⑤加入![]() 固体;⑥向
固体;⑥向![]() 中通入HCl气体。 其中可提高
中通入HCl气体。 其中可提高![]() 生成速率的措施有
生成速率的措施有
A.①③④B.①③⑥C.②④⑤D.①④⑥
【答案】B
【解析】
铁片与稀硫酸反应制取氢气的实质为:Fe+2H+=Fe2++H2↑。
①不用铁片,改用铁粉,可增大反应物的接触面积,提高生成氢气的速率,①符合;
②加入少量![]() 溶液,溶液总体积增大,H+浓度减小,生成氢气的速率减慢,②不符合;
溶液,溶液总体积增大,H+浓度减小,生成氢气的速率减慢,②不符合;
③加入少量![]() 固体,Fe和
固体,Fe和![]() 反应置换出Cu,形成原电池,生成氢气的速率加快,③符合;
反应置换出Cu,形成原电池,生成氢气的速率加快,③符合;
④常温下,浓硫酸将Fe钝化,不产生氢气,④不符合;
⑤加入![]() 固体,H+存在下NO3-具有强氧化性,Fe、H+、NO3-发生氧化还原反应不产生氢气,⑤不符合;
固体,H+存在下NO3-具有强氧化性,Fe、H+、NO3-发生氧化还原反应不产生氢气,⑤不符合;
⑥向![]() 中通入HCl气体,H+浓度增大,产生氢气的速率加快,⑥符合;
中通入HCl气体,H+浓度增大,产生氢气的速率加快,⑥符合;
综上所述,①③⑥能提高生成氢气的速率,B符合。
答案选B。

【题目】下表是元素周期表一部分,列出了九种元素在周期表中的位置:
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
1 | ① | |||||||
2 | ② | ③ | ④ | ⑤ | ||||
3 | ⑥ | ⑦ | ⑧ | ⑨ |
请用化学用语回答下列问题
(1)在上述元素中,金属性最强的是____________。
(2)①~⑨中元素最高价氧化物对应的水化物中酸性最强的是________(填物质化学式)。写出⑥和⑧的最高价氧化物对应的水化物反应的离子方程式 _______________________________。
(3)只由④形成的18电子微粒的电子式 _______________。
(4)写出由①和③形成的离子化合物的化学式 ____________________________。
(5)用电子式表示⑦和⑨形成的化合物的形成过程_________________________________。
(6)表中元素③和⑤可形成一种相对分子质量为66的共价化合物Y,Y分子中各原子均达到“8电子稳定结构”,Y的结构式 _________________。
【题目】某强酸性无色溶液中可能含下表离子中的若干种离子。
阳离子 | Mg2+、NH4+、Ba2+、Al3+、Fe2+ |
阴离子 | SiO32-、MnO4-、Cl-、NO3-、SO32- |
实验I :取少量该试液进行如下实验。
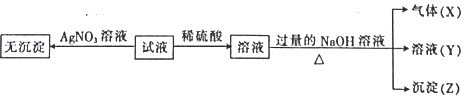
实验Ⅱ:为了进一步确定该溶液的组成,取100 mL原溶液,向该溶液中滴加1 mol L-l的 NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。

回答下列问题:
(1)不进行实验就可以推断出,上表中的离子一定不存在的有___________种。
(2)通过实验I可以确定该溶液中一定存在的阴离子是_____________。检验气体X的方法是______________________;沉淀Z的化学式为_________________。
(3)写出实验Ⅱ的图象中BC段对应的离子方程式:_____________________________________。
(4) A点对应的固体质量为__________g。
(5)通过上述信息,推算该溶液中阴离子的浓度为______________mol L-l。