题目内容
【题目】某强酸性无色溶液中可能含下表离子中的若干种离子。
阳离子 | Mg2+、NH4+、Ba2+、Al3+、Fe2+ |
阴离子 | SiO32-、MnO4-、Cl-、NO3-、SO32- |
实验I :取少量该试液进行如下实验。
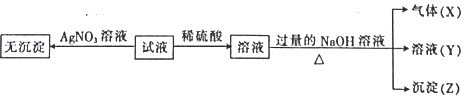
实验Ⅱ:为了进一步确定该溶液的组成,取100 mL原溶液,向该溶液中滴加1 mol L-l的 NaOH溶液,产生沉淀的质量与氢氧化钠溶液体积的关系如图所示。

回答下列问题:
(1)不进行实验就可以推断出,上表中的离子一定不存在的有___________种。
(2)通过实验I可以确定该溶液中一定存在的阴离子是_____________。检验气体X的方法是______________________;沉淀Z的化学式为_________________。
(3)写出实验Ⅱ的图象中BC段对应的离子方程式:_____________________________________。
(4) A点对应的固体质量为__________g。
(5)通过上述信息,推算该溶液中阴离子的浓度为______________mol L-l。
【答案】 4 NO3- 用镊子夹一块湿润的红色石蕊试纸靠近气体X,试纸变蓝 Mg(OH)2 Al(OH)3+OH-==AlO2-+2H2O 0.136 0.08
【解析】溶液无色,则不存在亚铁离子、高锰酸根离子;溶液显酸性,则不存在硅酸根离子和亚硫酸根离子;该溶液与硝酸银溶液混合后无沉淀生成,则不存在氯离子,因此一定含有硝酸根离子;该溶液与稀硫酸反应得不到沉淀,说明不存在钡离子,所得溶液与过量的氢氧化钠溶液混合生成气体X、溶液Y和沉淀Z,X是氨气,一定含有铵根离子;沉淀一定是氢氧化镁,含有镁离子;根据图像可知开始时氢氧化钠首先中和氢离子,然后沉淀金属阳离子,沉淀达到最大值后开始与铵根结合生成氨气,然后沉淀开始减少,最后不再发生变化,所以溶解的沉淀一定是氢氧化铝,含有铝离子。则
(1)根据以上分析可知不进行实验就可以推断出上表中的离子一定不存在的有4种,即亚铁离子、硅酸根离子、高锰酸根离子和亚硫酸根离子。(2)通过实验I可以确定该溶液中一定存在的阴离子是NO3-。氨气是碱性气体,检验氨气的方法是用镊子夹一块湿润的红色石蕊试纸靠近气体X,试纸变蓝;根据以上分析可知沉淀Z的化学式为Mg(OH)2。(3)实验Ⅱ的图象中BC段发生氢氧化铝的溶解,对应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O。(4)A点消耗氢氧化钠6mL,则与金属阳离子反应的氢氧化钠是5mL,物质的量是0.005mol。溶解氢氧化铝消耗氢氧化钠是1mL,物质的量是0.001mol,所以生成的氢氧化铝是0.001mol,则与镁离子反应的氢氧化钠是0.002mol,氢氧化镁是0.001mol,所以对应的固体质量为0.001mol×(58+78)g/mol=0.136g。(5)与氢离子反应的氢氧化钠是1mL,物质的量是0.001mol,即氢离子是0.001mol。与铵根反应的氢氧化钠是2mL,物质的量是0.002mol,即铵根是0.002mol,根据溶液显电中性可知硝酸根的物质的量是0.001mol+0.002mol+0.001mol×3+0.001mol×2=0.008mol,所以该溶液中阴离子的浓度为0.008mol÷0.1L=0.08mol L-l。

【题目】根据所学知识填空。
(1)与标准状况下4.48L CO2中所含氧原子数目相同的水的质量是g;
(2)V L Fe2(SO4)3溶液中含Fe3+m g,则溶液中SO42﹣的物质的量浓度为mol/L;
(3)9.2g氮的氧化物(NOx)中含氮原子0.2mol,则x的数值为;
(4)0.4mol某气体的体积为9.8L,则该气体的摩尔体积为 , 气体所处的条件(填“是”或“不是”)标准状况.
(5)下列是常用的中和胃酸的药物:
药名 | 胃舒平 | 达喜 |
有效成分的化学式 | Al(OH)3 | Al2Mg6(OH)16CO34H2O |
相对分子质量 | 78 | 530 |
每片含有效成份的药量 | 0.245g | 0.5g |
估算10片胃舒平和5片达喜,含铝的物质的量较多的是 .

