题目内容
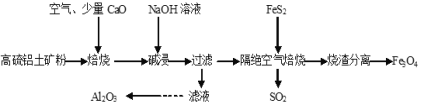
【题目】以高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,生产氧化铝并获得Fe3O4的部分工艺流程如图,下列叙述错误的是( )
A.烧渣分离可以选择用磁铁将烧渣中的Fe3O4分离出来
B.隔绝空气焙烧时理论上反应消耗的n(FeS2)∶n(Fe2O3)=1∶5
C.向滤液中通入过量CO2、过滤、洗涤、灼烧沉淀可制得Al2O3
D.加入CaO可以减少SO2的排放同时生成建筑材料CaSO4
【答案】B
【解析】
由流程可知,高硫铝土矿(主要成分为Al2O3、Fe2O3,还含有少量FeS2)为原料,通入空气焙烧时,因为含有少量FeS2,会产生二氧化硫,加入氧化钙达到吸收二氧化硫的目的,防止二氧化硫排放污染空气,焙烧产物经过氢氧化钠溶液碱浸,三氧化二铝与氢氧化钠反应生成偏铝酸钠,过滤后,滤液中通入过量二氧化碳,偏铝酸根与二氧化碳、水反应生成氢氧化铝沉淀,洗涤后灼烧氢氧化铝即可生产三氧化二铝;碱浸过程中,三氧化二铁不与氢氧化钠反应,过滤后留在滤渣中,加入FeS2与三氧化二铁在隔绝空气的条件下反应生成二氧化硫和四氧化三铁,利用四氧化三铁的磁性实现其与烧渣的分离。据此分析解答。
A.Fe3O4有磁性,可以用磁铁将Fe3O4从烧渣中分离出来,故A正确;
B.隔绝空气焙烧,FeS2与Fe2O3反应,生成SO2和Fe3O4,反应方程式为:FeS2+16Fe2O3 ![]() 11Fe3O4+2SO2↑,由方程式可知n(FeS2)∶n(Fe2O3)=1∶16,故B错误;
11Fe3O4+2SO2↑,由方程式可知n(FeS2)∶n(Fe2O3)=1∶16,故B错误;
C.滤液中含有AlO2-,通入过量CO2,发生反应:AlO2-+CO2+2H2O=Al(OH)3↓+ HCO3-,生成Al(OH)3沉淀,经过过滤、洗涤后得到Al(OH)3,再灼烧Al(OH)3,反应为:2Al(OH)3 ![]() +3H2O,即可制得Al2O3,故C正确;
+3H2O,即可制得Al2O3,故C正确;
D.铝土矿中含有FeS2,FeS2焙烧生成SO2,CaO与SO2、O2反应:2CaO+2SO2+O2=2CaSO4,CaSO4可用于建筑材料,故D正确;
故选B。

 名校课堂系列答案
名校课堂系列答案
