题目内容
下列关于下图所示原电池装置的叙述中,正确的是( ) 
| A.铜片作负极,质量逐渐减小 | B.溶液的pH逐渐减小 |
| C.电流从锌片经导线流向铜片 | D.氢离子在铜片表面被还原 |
D
解析试题分析:在如图所示原电池装置中,Zn是负极,发生氧化反应,Zn失去电子变为离子进入溶液,故质量会减轻; Cu是正极,在正极上氢离子得到电子被还原,发生还原反应;电子由Zn经过外电路到Cu电极,则电流则由Cu经过外电路到锌;由于溶液中的H+不断放电,所以H+的浓度不断降低,溶液的pH逐渐增大。因此正确的说法是D。
考点:考查原电池的各种原理的知识。

练习册系列答案
相关题目
如图是一种应用广泛的锂电池,LiPF6是电解质,SO(CH3)2是溶剂,反应原理是4Li+FeS2=Fe+2Li2S。下列说法不正确的是
| A.可以用水代替SO(CH3)2做溶剂 | B.电子移动方向是由a极流向b极 |
| C.该装置将化学能转化为电能 | D.b极反应式是FeS2+4Li++4e-=Fe+2Li2S |
在25ºC时,将两根铂电极插入一定量的硫酸钠饱和溶液中进行电解,当电路中有a mol电子转移时,溶液中析出mg Na2SO4 ·10 H2 O晶体。若温度不变,在剩余溶液中溶质的质量分数为
A.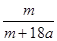 ×100% ×100% | B. ×100% ×100% |
C. ×100% ×100% | D.71m/161(m+9a) ×100% |
一种氢氧燃料电池用30%KOH溶液为电解质溶液,有关这种电池的说法中错误的是
| A.H2在负极发生氧化反应 | B.供电时的总反应为:2H2 + O2 = 2H2O |
| C.产物为无污染的水,属于环境友好电池 | D.负极反应为:H2 - 2e- = 2H+ |
利用电解法可将含有Fe、Zn、Ag、Pt等杂质的粗铜提纯,下列叙述正确的是
| A.电解时以精铜作阳极 |
| B.电解时阴极发生还原反应 |
| C.粗铜连接电源负极,其电极反应是Cu =Cu2+ + 2e- |
| D.电解结束,电解槽底部会形成含少量Ag、Pt等金属的阳极泥 |
观察下列几个装置示意图,有关叙述正确的是
| A.装置①中阳极上析出红色固体 |
| B.装置②的待镀铁制品应与电源负极相连 |
| C.装置③中外电路电子由b极流向a极 |
| D.装置④的离子交换膜允许阳离子、阴离子、水分子自由通过 |
据报道,美国正在研究的锌电池可能取代目前广泛使用的铅蓄电池。锌电池具有容量大、污染少等优点。电池反应为2Zn+O2=2ZnO,原料为锌粒、电解液和空气。下列叙述正确的是
| A.锌为正极,空气进入负极反应 |
| B.负极反应为Zn+2OH--2e-=ZnO+H2O |
| C.正极发生氧化反应 |
| D.电解液肯定是强酸 |
某氢氧燃料电池的电解液是热的KOH溶液,在正极上氧气被还原,在负极上氢气被氧化,下列有关该电池的叙述正确的是
| A.负极反应式为:H2+2OH- -2e- =2H2O |
| B.正极反应式为:O2 +4H+十4e- =2H2O |
| C.工作一段时间后,KOH溶液的浓度不变 |
| D.电池工作时,电子由正极通过外电路流向负极 |
