题目内容
19.下列化学反应的离子方程式正确的是( )| A. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| C. | 向小苏打溶液中加入过量的澄清石灰水:CO32-+Ca2+═CaCO3↓ | |
| D. | 向FeCl3溶液中加入Na:3Na+Fe3+═Fe+3Na+ |
分析 A.在稀氨水中通入过量CO2生成碳酸氢铵;
B.发生氧化还原反应生成硫酸钙;
C.向小苏打溶液中加入过量的澄清石灰水生活碳酸钙和水;
D.钠先和水反应生成氢氧化钠和氢气,进而生成氢氧化铁沉淀.
解答 解:A.在稀氨水中通入过量CO2生成碳酸氢铵,反应的离子方程式为NH3•H2O+CO2═NH4++HCO3-,故A正确;
B.向次氯酸钙溶液中通入少量SO2的离子反应为Ca2++ClO-+SO2+H2O═CaSO4↓+Cl-+2H+,故B错误;
C.向小苏打溶液中加入过量的澄清石灰水生活碳酸钙和水,反应的离子方程式为HCO3-+OH-+Ca2+═CaCO3↓+H2O,故C错误;
D.向FeCl3溶液中加入Na,反应的离子方程式为6Na+2Fe3++6H2O=2Fe(OH)3↓+6Na++3H2↑,故D错误.
故选A
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生反应及离子反应的书写方法为解答的关键,侧重氧化还原反应、复分解反应的离子反应及分析与应用能力的考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
10.盐酸、醋酸和碳酸氢钠是生活中常见的物质.下列表述正确的是( )
| A. | 10mL0.10mol•L-1CH3COOH溶液加入等物质的量的NaOH后,溶液中离子的浓度由大到小的顺序是:c(Na+)>c(CH3COO-)>c(OH-)>c(H+) | |
| B. | NaHCO3溶液中:c(H+)+c(H2CO3)=c(OH-) | |
| C. | 在NaHCO3溶液中加入等物质的量的NaOH,溶液中的阴离子只有CO32-和OH- | |
| D. | 中和体积与pH都相同的HCl溶液和CH3COOH溶液所消耗的NaOH的物质的量相同 |
7.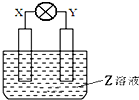 如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是( )
如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是( )
 如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是( )
如图所示装置中,观察到电流计指针偏转,X棒变重,Y棒变轻,由此判断下表中所列X、Y、Z物质,其中可以成立的是( )| X | Y | Z | |
| A | 锌 | 铜 | 稀硫酸溶液 |
| B | 铜 | 铁 | 稀盐酸 |
| C | 锌 | 铜 | 硝酸银溶液 |
| D | 碳 | 锌 | 硝酸铜溶液 |
| A. | 锌做负极溶解X电极变轻,错误 | |
| B. | 铁做负极失电子溶解变轻,X电极生成氢气不会变重,错误 | |
| C. | 锌做负极溶解X电极变轻,错误 | |
| D. | 锌做负极失电子发生氧化反应Y棒变轻,碳做正极溶液中铜离子析出使X极变重,正确 |
14.下列有关化学用语使用不正确的是( )
| A. | 氯原子的原子结构示意图: | |
| B. | C2H4的结构简式:CH2CH2 | |
| C. | 原子核内有10个中子的氧原子:${\;}_{8}^{18}$O | |
| D. | CH4 分子的结构模型: |
9.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 1.0 L 1.0 mol•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| C. | 常温常压下,92 g NO2和N2O4的混合气体中含有的原子总数为6NA | |
| D. | 标准状况下,22.4 L氨水含有NA个NH3分子 |

 的名称2,3-二甲基戊烷
的名称2,3-二甲基戊烷