题目内容
9.设NA为阿伏加德罗常数的值,下列叙述正确的是( )| A. | 1.0 L 1.0 mol•L-1的NaAlO2水溶液中含有的氧原子数为2NA | |
| B. | 25℃时pH=13的NaOH溶液中含有OH-的数目为0.1NA | |
| C. | 常温常压下,92 g NO2和N2O4的混合气体中含有的原子总数为6NA | |
| D. | 标准状况下,22.4 L氨水含有NA个NH3分子 |
分析 A、NaAlO2水溶液中除了NaAlO2中含有氧原子,水中也含有氧原子;
B、溶液体积不明确;
C、NO2和N2O4的最简式均为NO2;
D、标况下,氨水是液体.
解答 解:A、NaAlO2水溶液中除了NaAlO2中含有氧原子,水中也含有氧原子,故1.0 L 1.0 mol•L-1的NaAlO2水溶液中含有的氧原子数大于2NA,故A错误;
B、溶液体积不明确,故溶液中的氢氧根的个数无法计算,故B错误;
C、NO2和N2O4的最简式均为NO2,故92g混合物中的NO的物质的量n=$\frac{92g}{46g/mol}$=2mol,故含有6mol原子即6NA个,故C正确;
D、标况下,氨水是液体,故不能根据气体摩尔体积来计算其物质的量,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,掌握物质的量的计算公式和物质结构是解题关键,难度不大.

练习册系列答案
相关题目
19.下列化学反应的离子方程式正确的是( )
| A. | 在稀氨水中通入过量CO2:NH3•H2O+CO2═NH4++HCO3- | |
| B. | 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO | |
| C. | 向小苏打溶液中加入过量的澄清石灰水:CO32-+Ca2+═CaCO3↓ | |
| D. | 向FeCl3溶液中加入Na:3Na+Fe3+═Fe+3Na+ |
20.20gA物质和14gB物质恰好完全反应,生成8.8gC物质、3.6gD物质和0.2molE物质,则E物质的摩尔质量为( )
| A. | 100 g•mol-1 | B. | 108 g•mol-1 | C. | 55 g•mol-1 | D. | 96 g•mol-1 |
17.下列物质既含有离子键又含有极性键和非极性键的是( )
| A. | KOH | B. | H2O2 | C. | CH3COONa | D. | NH4Cl |
1.pH=1酸溶液和pH=13碱溶液等体积混合后pH正确的是( )
| A. | 混合溶液的pH值应等于7 | |
| B. | 如果酸是强酸,则pH一定小于7 | |
| C. | 如果碱是强碱,则pH一定不大于7 | |
| D. | 如果混合液的pH大于7,则碱一定为强碱 |
18.一定条件下进行反应:A(g)?B(g)+C (g),向2.0L恒容密闭容器中充入1.0mol A(g),经过一段时间后达到平衡.反应过程中测得的有关数据如表:
下列说法正确的是( )
| t/s | 0 | 2 | 4 | 6 | 8 |
| n(B)/mol | 0 | 0.30 | 0.39 | 0.40 | 0.40 |
| A. | 反应前2min的平均速率v(B)=0.15 mol/(L•min) | |
| B. | 保持其他条件不变,升高温度,平衡时c(B)=0.22 mol•L-1,则反应的△H<0 | |
| C. | 保持其他条件不变,起始向容器中充入2.0 mol A,反应达到平衡时C的体积分数减小 | |
| D. | 保持其他条件不变,增大该反应体系的压强,平衡左移,反应的平衡常数K减小 |
19.下列事实与胶体性质无关的是( )
| A. | 向豆浆中加入盐卤做豆腐 | |
| B. | 钢笔使用不同牌子的墨水堵塞 | |
| C. | 一束平行光线射入蛋白质溶液里,从侧面可以看到一束光亮的通路 | |
| D. | 向石灰水中通入二氧化碳气体产生白色浑浊 |
 某同学为探究元素周期表中元素性质的递变规律,设计了如下实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下实验.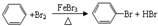 ,预测该芳香烃能(填“能”或“不能”)发生该类反应.
,预测该芳香烃能(填“能”或“不能”)发生该类反应.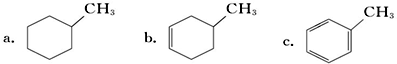
 c.
c.