题目内容
在常见的非金属及其化合物中:
(1)晶体硅的导电性介于导体和绝缘体之间,是良好的 材料;硅酸钠水溶液俗称为 ,是制备硅胶和木材防火剂的原料;陶瓷、 、水泥等硅酸盐产品是使用量最大的无机非金属材料.
(2)氯元素是重要的“成盐元素”,将氯气通入NaOH溶液中可以得到漂白液,反应的离子方程式是 ;漂白液有效成分的化学式为 .
(3)水是常见的非金属元素化合物,请按要求写出下列水参加的反应的化学方程式.
①水只作氧化剂:
②NO2气体通入水中:
③水既作氧化剂又作还原剂: .
(1)晶体硅的导电性介于导体和绝缘体之间,是良好的
(2)氯元素是重要的“成盐元素”,将氯气通入NaOH溶液中可以得到漂白液,反应的离子方程式是
(3)水是常见的非金属元素化合物,请按要求写出下列水参加的反应的化学方程式.
①水只作氧化剂:
②NO2气体通入水中:
③水既作氧化剂又作还原剂:
考点:硅和二氧化硅,氧化还原反应,氯气的化学性质,氮的氧化物的性质及其对环境的影响
专题:元素及其化合物
分析:(1)晶体硅是良好的半导体材料;
硅酸钠水溶液俗称为水玻璃;
陶瓷、玻璃、水泥等硅酸盐产品是使用量最大的无机非金属材料;
(2)氯气和NaOH溶液反应生成氯化钠、次氯酸钠和水,漂白液有效成分为NaClO;
(3)①水只作氧化剂说明水中的氢元素化合价降低;
②NO2气体通入水中,生成硝酸和一氧化氮;
③若水既是氧化剂又是还原剂,则水中H、O元素的化合价在反应前后发生变化,应生成氧气和氢气.
硅酸钠水溶液俗称为水玻璃;
陶瓷、玻璃、水泥等硅酸盐产品是使用量最大的无机非金属材料;
(2)氯气和NaOH溶液反应生成氯化钠、次氯酸钠和水,漂白液有效成分为NaClO;
(3)①水只作氧化剂说明水中的氢元素化合价降低;
②NO2气体通入水中,生成硝酸和一氧化氮;
③若水既是氧化剂又是还原剂,则水中H、O元素的化合价在反应前后发生变化,应生成氧气和氢气.
解答:
解:(1)晶体硅的导电性介于导体和绝缘体之间,是良好的半导体材料;硅酸钠水溶液俗称为水玻璃,是制备硅胶和木材防火剂的原料;陶瓷、玻璃、水泥等硅酸盐产品是使用量最大的无机非金属材料;
故答案为:半导体;水玻璃;玻璃;
(2)氯气和NaOH溶液反应生成氯化钠、次氯酸钠和水,离子方程式为Cl2+2OH-═Cl-+ClO-+H2O,漂白液有效成分为NaClO,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;NaClO;
(3)①水只作氧化剂说明水中的氢元素化合价降低,方程式为:2Na+2H2O=2NaOH+H2↑,
故答案为:2Na+2H2O=2NaOH+H2↑;
②NO2气体通入水中,生成硝酸和一氧化氮,方程式为:3NO2+H2O=2HNO3+NO,
故答案为:3NO2+H2O=2HNO3+NO;
③若水既是氧化剂又是还原剂,则水中H、O元素的化合价在反应前后发生变化,应生成氧气和氢气,方程式为:2H2O
2H2↑+O2↑,
故答案为:2H2O
2H2↑+O2↑.
故答案为:半导体;水玻璃;玻璃;
(2)氯气和NaOH溶液反应生成氯化钠、次氯酸钠和水,离子方程式为Cl2+2OH-═Cl-+ClO-+H2O,漂白液有效成分为NaClO,
故答案为:Cl2+2OH-=Cl-+ClO-+H2O;NaClO;
(3)①水只作氧化剂说明水中的氢元素化合价降低,方程式为:2Na+2H2O=2NaOH+H2↑,
故答案为:2Na+2H2O=2NaOH+H2↑;
②NO2气体通入水中,生成硝酸和一氧化氮,方程式为:3NO2+H2O=2HNO3+NO,
故答案为:3NO2+H2O=2HNO3+NO;
③若水既是氧化剂又是还原剂,则水中H、O元素的化合价在反应前后发生变化,应生成氧气和氢气,方程式为:2H2O
| ||
故答案为:2H2O
| ||
点评:本题考查硅和二氧化硅的用途、氯气的化学性质、氧化还原反应方程式的书写等,综合性较强,难度中等.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
下列分子式对应的结构式,从价键的成键情况看不合理的是( )
A、CH3N: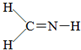 |
B、CH4Si: |
C、CH4S: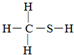 |
D、CH2SeO: |
下列微粒中能影响水的电离平衡,且使水的电离平衡向左移动的是( )
| A、SO42- |
| B、Cl- |
| C、Na+ |
D、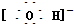 |
下列依据相关实验得出的结论正确的是( )
| A、向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定是碳酸盐溶液 |
| B、向某溶液中滴加KSCN溶液,溶液不变色,滴加氯水后溶液显红色,该溶液中一定含Fe2+ |
| C、将某气体通入淀粉碘化钾溶液中,溶液变蓝,该气体一定是氯气 |
| D、用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 |
下列有关说法正确的是( )
| A、使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 |
| B、化学反应有新物质生成,并遵循质量守恒定律和能量守恒定律 |
| C、HCl和NaOH反应的中和热△H=-57.3kJ?mol-1,则H2SO4和Ca(OH)2反应的中和热△H=-114.6kJ?mol-1 |
| D、500℃、300MPa下,将0.5mol N2和1.5mol H2置于密闭容器中充分反应生成NH3(g),放热19.3kJ,其热化学方程式为N2(g)+3H2(g)?2NH3(g)△H=-38.6kJ?mol-1 |
常温下,下列溶液肯定呈酸性的是( )
| A、与金属铁反应放出氢气 |
| B、溶液中含有H+ |
| C、与金属铝反应放出氢气 |
| D、滴入酚酞试液后,溶液呈无色 |

 研究性学习小组进行溴乙烷的制备的相关探究实验.
研究性学习小组进行溴乙烷的制备的相关探究实验.