题目内容
3.科学研究发现纳米级的Cu2O可作为太阳光分解水的催化剂.Ⅰ四种制取Cu2O的方法
(a)用炭粉在高温条件下还原CuO制备Cu2O;
(b)用葡萄糖还原新制的Cu(OH)2悬浊液制备Cu2O;
(c)电解法制备Cu2O.原理如右图所示反应为:2Cu+H2O=Cu2O+H2↑,则铜作为阳极;
(d)最新实验研究加热条件下用液态肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时放出N2和水蒸气.该制法的化学方程式为4Cu(OH)2+N2H4 $\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+N2+6H2O.
Ⅱ用制得的Cu2O进行催化分解水的实验Cu2O光照
(1)一定温度下,在2L密闭容器中加入纳米级Cu2O并通入10.0mol水蒸气,发生反应:
2H2O(g)?2H2(g)+O2(g)△H=+484kJ•mol-1
T1温度下不同时段产生O2的量见下表:
| 时间/min | 20 | 40 | 60 | 80 |
| n(O2)/mol | 1.0 | 1.6 | 2.0 | 2.0 |
(2)用以上四种方法制得的Cu2O在某相同条件下分别对四份 相同质量的水催化分解,
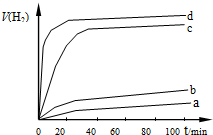 产生的氢气经干燥装置并用针筒收集;V(H2)随时间t变化如右图所示.下列叙述正确的是BC(双选题).
产生的氢气经干燥装置并用针筒收集;V(H2)随时间t变化如右图所示.下列叙述正确的是BC(双选题).A.d方法制得的Cu2O能使水剧烈分解并放出热量
B.d方法制得的Cu2O颗粒最小,表面活性大,所以催化效果明显.
C. c、d 产生的氢气总体积不同可能和水的蒸发有关
D. d方法制得的Cu2O作催化剂时,水的平衡转化率最高.
分析 Ⅰ.(b)葡萄糖[CH2OH(CHOH)4CHO]与新制的Cu(OH)2在加热条件下发生氧化还原反应生成葡萄糖酸和氧化亚铜;
(c)阳极发生氧化反应,根据化合物的变化判断;
(d)根据反应物和生成物结合质量守恒书写化学方程式;
Ⅱ.(1)根据化学反应速率之比等于计算数之比计算反应速率,达平衡时,生成氧气0.002mol,根据热化学方程式计算;
(2)根据图象曲线的变化趋势判断,曲线斜率越大,反应速率越大,温度升高,斜率逐渐减小,以此解答.
解答 解:I.(b)葡萄糖[CH2OH(CHOH)4CHO]与新制的Cu(OH)2在加热条件下发生氧化还原反应生成葡萄糖酸和氧化亚铜,
故答案为:新制的Cu(OH)2;
(c)阳极发生氧化反应,由方程式可知Cu被氧化生成Cu2O,
故答案为:阳;
(d)用肼(N2H4)还原新制Cu(OH)2可制备纳米级Cu2O,同时放出N2,反应的方程式为4Cu(OH)2+N2H4 $\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+N2+6H2O,
故答案为:4Cu(OH)2+N2H4 $\frac{\underline{\;\;△\;\;}}{\;}$2Cu2O+N2+6H2O;
Ⅱ.(1)由表中数据可知前20min时v(O2)=$\frac{\frac{0.0010mol}{2L}}{20min}$=2.5×10-5 mol.L-1.min -1,
则v(H2O)=2v(O2)=5.0×10-5 mol.L-1.min -1,
该反应的平衡常数表达式K=$\frac{{c}^{2}({H}_{2})•c({O}_{2})}{{c}^{2}({H}_{2}O)}$,平衡时c(H2O)=3mol.L-1,c(O2)=1mol.L-1,c(H2)=2mol.L-1,所以K=$\frac{{2}^{2}×1}{{3}^{2}}$=0.44>0.4,由于该反应是吸热反应,升高温度,平衡正向移动,K值增大,所以T1>T2,
故答案为:5.0×10-5 mol.L-1.min -1;$\frac{{c}^{2}({H}_{2})•c({O}_{2})}{{c}^{2}({H}_{2}O)}$;>;
(2)A.催化剂能加快反应速率,但不能改变反应的热效应,故A错误;
B.根据图中产生氢气的速率可以看出,d方法制得的Cu2O颗粒最小,表面活性大,所以催化效果明显,故B正确;
C. c、d中理论上水和氢气的关系是相同的,实际上c、d产生的氢气总体积不同可能和水的蒸发有关,故C正确;
D. 催化剂能加快反应速率,但不能改变反应的平衡转化率,故D错误,
故选BC.
点评 本题考查较为综合,涉及氧化亚铜的制备方案、电解、化学平衡以及反应速率的影响等知识,侧重于学生的分析能力的考查,为高考常见题型,难度中等.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案| A. | 单质分子中可能不含化学键 | |
| B. | 含有离子键的化合物一定是离子化合物 | |
| C. | 含有极性键的分子一定是极性分子 | |
| D. | 含有共价键的化合物不一定是共价化合物 |
H+(aq)+OH-(aq)=H2O(l);△H=-57.3k kJ•mol-1,
又知:CH3COOH(aq)+NaOH(aq)=CH3COONa(aq)+H2O(l);△H=-Q1kJ•mol-1,
$\frac{1}{2}$H2SO4(浓)+$\frac{1}{2}$Ba(OH)2(aq)=$\frac{1}{2}$BaSO4(aq)+H2O(l);△H=-Q2 kJ•mol-1
HNO3(aq)+KOH(aq)═KNO3(aq)+H2O(l);△H=-Q3 kJ•mol-1,
上述反应均为溶液中的反应,则Q1、Q2、Q3的大小关系是( )
| A. | Q2>Q3>Q1 | B. | Q2>Q1>Q3 | C. | Q1=Q2=Q3 | D. | Q2=Q3>Q1 |
| A. | 增大反应物用量 | B. | 使用催化剂 | C. | 增大体系压强 | D. | 升高温度 |
| A. | 向红褐色的Fe(OH)3固体中加入过量盐酸 | |
| B. | 等物质的量浓度、等体积的(NH4)2SO4与BaCl2溶液 | |
| C. | 等物质的量的NaHCO3与Na2O2固体 | |
| D. | 向NaBr溶液中通入过量氯气 |
| A. | Ca(HCO3)2溶液中加入过量NaOH溶液Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| B. | SO2通入溴水中SO2+Br2+2H2O═4H++2Br-+SO42- | |
| C. | 泡沫灭火器原理:2Al3++3CO32-+3H2O═2Al(OH)3↓+3CO2↑ | |
| D. | FeO与稀HNO3反应FeO+2H+═Fe2++H2O |
| A. | HNO3在反应中表现氧化性 | |
| B. | C在反应中被还原 | |
| C. | HNO3在反应中失去电子 | |
| D. | 1 mol 氧化剂在反应中得到4 mol电子 |
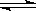 N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是( )
N2O4(g)达到平衡后,慢慢压缩气体体积,下列叙述正确的是( )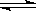 2SO3.当反应进行到4min时,测得此时SO2为0.4mol,那么反应进行到2min时,密闭容器中SO2物质的量是( )
2SO3.当反应进行到4min时,测得此时SO2为0.4mol,那么反应进行到2min时,密闭容器中SO2物质的量是( )