题目内容
9.向碘化银饱和溶液中加入饱和氯化银溶液出现沉淀后,各离子浓度关系是c(Cl-)>c(Ag+)>c(I-).分析 碘化银饱和溶液中存在溶解平衡:AgI(s)?Ag+(aq)+I-(aq),由于AgI的溶解度小于AgCl,加入饱和氯化银溶液后,导致c(Ag+)增大,AgI 的沉淀溶解平衡向左移动,析出AgI沉淀后,成为AgI的饱和溶液,则:c(Ag+)>c(I-),且c(Cl-)最大,据此判断各离子浓度大小.
解答 解:碘化银饱和溶液中存在溶解平衡:AgI(s)?Ag+(aq)+I-(aq),且AgI的溶解度小于AgCl,
加入饱和氯化银溶液后,c(Ag+)增大,AgI 的沉淀溶解平衡向左移动,析出AgI沉淀后,成为AgI的饱和溶液,则:c(Ag+)>c(I-),
此时c(Cl-)最大,溶液中离子浓度大小为:c(Cl-)>c(Ag+)>c(I-),
故答案为:c(Cl-)>c(Ag+)>c(I-).
点评 本题考查了离子浓度大小比较,题目难度中等,明确难溶物溶解平衡及其影响为解答关键,试题培养了学生的分析能力、理解能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
19.下列气体既能用浓硫酸干燥又能用碱石灰干燥的是( )
| A. | SO2 | B. | NH3 | C. | N2 | D. | CO2 |
20.根据下列实验或实验操作和现象,所得结论正确的是( )
| 实验或实验操作 | 现象 | 实验结论 | |
| A | 用大理石和盐酸反应制取CO2 气体,立即通入一定浓度的Na2SiO3溶液中 | 出现白色沉淀 | H2CO3的酸性比H2SiO3的酸性强 |
| B | 向某溶液先滴加硝酸酸化,再滴加BaCl2溶液 | 出现白色沉淀 | 原溶液中含有SO42-、SO32-、HSO3-中的一种或几种 |
| C | 将纯Zn片与纯Cu片用导线连接,浸入到稀硫酸溶液中 | Cu片表面产生大量气泡 | 金属性:Zn>Cu |
| D |  | 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性: Cl2>Br2>I2 |
| A. | A | B. | B | C. | C | D. | D |
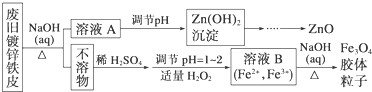
12.已知废旧干电池中的填充物主要有二氧化锰、炭黑、氯化锌、氯化铵、淀粉糊、Mn2O3、ZnO、FeO、汞的化合物等.某实验小组的同学拟回收废旧电池中的部份物质,主要操作流程如图:
下列说法不正确的是( )

下列说法不正确的是( )
| A. | 步骤①②的名称分别为溶解、过滤 | |
| B. | 步骤③中使用的化学仪器有酒精灯、三角架、泥三角、坩埚、玻璃棒 | |
| C. | 步骤①②③中都使用了玻璃棒,且三个操作中玻璃棒的作用不完全相同 | |
| D. | 步骤④的离子方程式为2Fe2++2H++H2O2=2Fe3++2H2O |
9.通常情况下,既能用浓硫酸干燥,又能用碱石灰干燥的气体是( )
| A. | NH3 | B. | Cl2 | C. | NO | D. | HCl |
 ,写出各步反应的化学方程式.
,写出各步反应的化学方程式.