题目内容
2. 食盐晶体如图所示,已知食盐的密度为ρg/cm3,NaCl摩尔质量Mg/mol,阿伏伽德罗常数为NA,则在食盐晶体里Na+和Cl-的间距大约是( )
食盐晶体如图所示,已知食盐的密度为ρg/cm3,NaCl摩尔质量Mg/mol,阿伏伽德罗常数为NA,则在食盐晶体里Na+和Cl-的间距大约是( )| A. | $\root{3}{\frac{2M}{p{N}_{A}}}$cm | B. | $\root{3}{\frac{M}{2p{N}_{A}}}$cm | C. | $\root{3}{\frac{2{N}_{A}}{pM}}$cm | D. | $\root{3}{\frac{M}{8p{N}_{A}}}$cm |
分析 该晶胞中钠离子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,氯离子个数=12×$\frac{1}{4}$+1=4,晶胞体积=$\frac{\frac{M}{{N}_{A}}×4}{ρ}$cm3,晶胞棱长=$\root{3}{\frac{\frac{M}{{N}_{A}}×4}{ρ}}$cm,食盐晶体里Na+和Cl-的间距为棱长的一半,据此分析解答.
解答 解:该晶胞中钠离子个数=8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,氯离子个数=12×$\frac{1}{4}$+1=4,晶胞体积=$\frac{\frac{M}{{N}_{A}}×4}{ρ}$cm3,晶胞棱长=$\root{3}{\frac{\frac{M}{{N}_{A}}×4}{ρ}}$cm,食盐晶体里Na+和Cl-的间距为棱长的一半=$\frac{1}{2}$×$\root{3}{\frac{\frac{M}{{N}_{A}}×4}{ρ}}$cm=$\root{3}{\frac{M}{2ρ{N}_{A}}}$cm,故选B.
点评 本题考查晶胞计算,为高频考点也是学习难点,侧重考查学生空间想象能力及计算能力,知道密度公式中各个字母含义是解本题关键,结合均摊法解答,题目难度中等.

练习册系列答案
相关题目
12.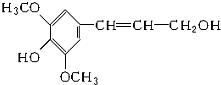 膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一--芥子醇结构简式如图所示,下列有关芥子醇的说法正确的是( )
膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一--芥子醇结构简式如图所示,下列有关芥子醇的说法正确的是( )
 膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一--芥子醇结构简式如图所示,下列有关芥子醇的说法正确的是( )
膳食纤维具有突出的保健功能,是人体的“第七营养素”.木质素是一种非糖类膳食纤维.其单体之一--芥子醇结构简式如图所示,下列有关芥子醇的说法正确的是( )| A. | 芥子醇分子中有两种含氧官能团 | |
| B. | 芥子醇分子中所有碳原子不可能在同一平面上 | |
| C. | 1 mol芥子醇与足量浓溴水反应,最多消耗3 mol Br2 | |
| D. | 芥子醇能发生的反应类型有氧化、取代、加成 |
13.NA为阿伏加德罗常数,下列有关说法正确的是( )
| A. | 常温下,7.8g固体Na2O2中,含有的阴阳离子总数为0.4NA | |
| B. | 4℃时,18g 2H216O中含有共用电子对数为2NA | |
| C. | 1 mol N5+含有的电子数为34NA | |
| D. | 用金属铁、Cu片、稀硫酸组成原电池,当金属铁质量减轻5.6g时,流过外电路的电子为0.3NA |
10.下列反应中属于吸热反应的是( )
| A. | 甲烷燃烧 | B. | Ba(OH)2•8H2O与NH4Cl反应 | ||
| C. | 铝片与盐酸反应 | D. | 氧化钙与水反应 |
17.等电子体之间往往具有相似的结构,N2O与CO2分子具有相似的结构(包括电子式);已知N2O分子中氧原子只与一个氮原子相连,下列说法合理的是( )
| A. | N2O为三角形分子 | |
| B. | N2O与CO2均不含非极性键 | |
| C. | N2O的电子式可表示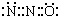 | |
| D. | N2O与SiO2为等电子体、具有相似的结构和相似性质 |
14.下列各组元素的原子序数中,其相应的元素原子能形成XY2型共价化合物的是( )
| A. | 3与8 | B. | 6与8 | C. | 1与16 | D. | 12与17 |
11.下列化学用语所表示的微粒中,不能与盐酸发生化学反应的是( )
| A. |  | B. | ${\;}_{11}^{23}$Na | C. | 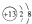 | D. | Mg |
 氧(O)、硫(S)、硒(Se)、碲(Te)为ⅥA族元素,请回答下列问题:
氧(O)、硫(S)、硒(Se)、碲(Te)为ⅥA族元素,请回答下列问题: 的沸点比
的沸点比 高,原因是对羟基苯甲醛分子间能形成氢键、邻羟基苯甲醛分子内能形成氢键.
高,原因是对羟基苯甲醛分子间能形成氢键、邻羟基苯甲醛分子内能形成氢键.

 .
.