题目内容
13.NA为阿伏加德罗常数,下列有关说法正确的是( )| A. | 常温下,7.8g固体Na2O2中,含有的阴阳离子总数为0.4NA | |
| B. | 4℃时,18g 2H216O中含有共用电子对数为2NA | |
| C. | 1 mol N5+含有的电子数为34NA | |
| D. | 用金属铁、Cu片、稀硫酸组成原电池,当金属铁质量减轻5.6g时,流过外电路的电子为0.3NA |
分析 A.1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总计3mol阴阳离子;
B.每个2H216O含有2对共用电子对,根据n=$\frac{m}{M}$计算2H216O的物质的量,再根据N=nNA计算共用电子对数目;
C.1个N5+含有34个电子;
D.铁在反应表现+2价,根据n=$\frac{m}{M}$计算铁物质的量,再根据N=nNA计算电子数目.
解答 解:A.由于1mol过氧化钠中含有2mol钠离子、1mol过氧根离子,总计3mol阴阳离子,7.8g过氧化钠的物质的量是0.1mol,总计含有0.3mol阴阳离子,含有阴阳离子总数为0.3NA,故A错误;
B.18g2H216O中含有共用电子对数为$\frac{18g}{20g/mol}$×2×NAmol-1=1.8NA,故B错误;
C.1个N5+含有34个电子,1 mol N5+含有的电子数为34NA,故C正确;
D.铁在反应表现+2价,当金属铁质量减轻5.6g时,流过外电路的电子数为$\frac{5.6g}{56g/mol}$×2×NAmol-1=0.2NA,故D错误;
故选:C.
点评 本题考查常用化学计量数的有关计算,注意注意物质的组成、结构、性质,熟练掌握公式的使用是解题关键,题目难度不大.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
3.已知:
①H2O(g)═H2O(l)△H=-Q1kJ.mol-1
②C2H5OH(g)═C2H5OH(1)△H=-Q2kJ.mol-1
③C2H5OH(g)═302(g)=2C02(g)+3H20(g)△H=-Q3 kJ.mol-1
下列判断正确的是( )
①H2O(g)═H2O(l)△H=-Q1kJ.mol-1
②C2H5OH(g)═C2H5OH(1)△H=-Q2kJ.mol-1
③C2H5OH(g)═302(g)=2C02(g)+3H20(g)△H=-Q3 kJ.mol-1
下列判断正确的是( )
| A. | 酒精的燃烧热AH=-Q3 kJ•mol-1 | |
| B. | 由③可知1molC2H5OH(g)的能量高于2molC02(g)和3 molH20(g)的总能量 | |
| C. | H20(g)→H20( 1)释放出了热量,所以该过程为放热反应 | |
| D. | 23g液体酒精完全燃烧生成C02(g)和H20( 1),释放热量为(0.5Q3-0.5Q2+1.5Q1)kJ |
4.下列叙述中正确的是( )
| A. | 液态HCl、固体NaCl均不导电,所以HCl和NaCl均是非电解质 | |
| B. | NH3、SO3的水溶液均导电,所以NH3、SO3均是电解质 | |
| C. | 常见的酸、碱和大部分盐都是强电解质 | |
| D. | 强电解质与弱电解质的本质区别,是其在水溶液中的电离程度不同 |
18. 共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量或形成1mol共价键所放出的能量.
共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量或形成1mol共价键所放出的能量.
(1)已知H-Cl键的键能为431.4kJ/mol,下列关于键能的叙述正确的是AD.
A.每生成1mol H-Cl键放出431.4kJ能量 B.每生成1mol H-Cl键吸收431.4kJ能量
C.每拆开1mol H-Cl键放出431.4kJ能量 D.每拆开1mol H-Cl键吸收431.4kJ能量
(2)参考下表中的数据,判断下列分子受热时最稳定的是A.
A.HF B.HCl C.HBr D.H2
(3)能用键能大小解释的是A.
A.氮气的化学性质比氧气稳定
B.常温常压下,溴呈液态,碘呈固态
C.稀有气体一般很难发生化学反应
D.硝酸易挥发而硫酸难挥发
(4)已知:4HCl+O2═2Cl2+2H2O,该反应中,4mol HCl被氧化,放出115.6kJ的热量.断开1mol H-O键与断开1mol H-Cl键所需能量相差约为31.9kJ.
 共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量或形成1mol共价键所放出的能量.
共价键都有键能之说,键能是指拆开1mol共价键所需要吸收的能量或形成1mol共价键所放出的能量.(1)已知H-Cl键的键能为431.4kJ/mol,下列关于键能的叙述正确的是AD.
A.每生成1mol H-Cl键放出431.4kJ能量 B.每生成1mol H-Cl键吸收431.4kJ能量
C.每拆开1mol H-Cl键放出431.4kJ能量 D.每拆开1mol H-Cl键吸收431.4kJ能量
(2)参考下表中的数据,判断下列分子受热时最稳定的是A.
| 化学键 | H-H | H-F | H-Cl | H-Br |
| 键能/kJ/mol | 436 | 565 | 431 | 368 |
(3)能用键能大小解释的是A.
A.氮气的化学性质比氧气稳定
B.常温常压下,溴呈液态,碘呈固态
C.稀有气体一般很难发生化学反应
D.硝酸易挥发而硫酸难挥发
(4)已知:4HCl+O2═2Cl2+2H2O,该反应中,4mol HCl被氧化,放出115.6kJ的热量.断开1mol H-O键与断开1mol H-Cl键所需能量相差约为31.9kJ.
5.下列各表中的数字代表的是原子序数,表中数字所表示的元素与它们在元素周期表中的位置相符的是( )
| A. |
| B. |
| C. |
| D. |
|
2. 食盐晶体如图所示,已知食盐的密度为ρg/cm3,NaCl摩尔质量Mg/mol,阿伏伽德罗常数为NA,则在食盐晶体里Na+和Cl-的间距大约是( )
食盐晶体如图所示,已知食盐的密度为ρg/cm3,NaCl摩尔质量Mg/mol,阿伏伽德罗常数为NA,则在食盐晶体里Na+和Cl-的间距大约是( )
 食盐晶体如图所示,已知食盐的密度为ρg/cm3,NaCl摩尔质量Mg/mol,阿伏伽德罗常数为NA,则在食盐晶体里Na+和Cl-的间距大约是( )
食盐晶体如图所示,已知食盐的密度为ρg/cm3,NaCl摩尔质量Mg/mol,阿伏伽德罗常数为NA,则在食盐晶体里Na+和Cl-的间距大约是( )| A. | $\root{3}{\frac{2M}{p{N}_{A}}}$cm | B. | $\root{3}{\frac{M}{2p{N}_{A}}}$cm | C. | $\root{3}{\frac{2{N}_{A}}{pM}}$cm | D. | $\root{3}{\frac{M}{8p{N}_{A}}}$cm |
3.在一密闭容器中进行反应2SO2+O2?2SO3,已知反应过程中某一时刻SO2、O2、SO3的浓度分别为2mol•L-1、1mol•L-1、2mol•L-1.当反应达到平衡时,容器内各物质的浓度可能为( )
| A. | SO2为4 mol•L-1、O2为2 mol•L-1 | B. | SO3为4 mol•L-1 | ||
| C. | SO2为2.5 mol•L-1 | D. | SO2、SO3为1.5 mol•L-1 |
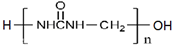 )可用于胶合板、刨花板等人造板材的生产及室内装修,但在使用过程中会释放出有毒物质,请写出合成该物质的单体的结构简式:CO(NH2)2、HCHO.
)可用于胶合板、刨花板等人造板材的生产及室内装修,但在使用过程中会释放出有毒物质,请写出合成该物质的单体的结构简式:CO(NH2)2、HCHO. )具有碱性.(选填“酸性”、“碱性”或“中性”)
)具有碱性.(选填“酸性”、“碱性”或“中性”)
 ,操作②的名称为重结晶.
,操作②的名称为重结晶. 转化为
转化为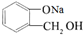 ,所选择的最佳试剂为H2O.
,所选择的最佳试剂为H2O. 为了验证铜与稀硝酸反应产生的是一氧化氮而不是氢气.某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;C中有足量的澄清石灰水,E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.
为了验证铜与稀硝酸反应产生的是一氧化氮而不是氢气.某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去).B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;C中有足量的澄清石灰水,E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.