题目内容
10.关于下列说法:①Fe(OH)3胶体和CuSO4溶液都是混合物;②BaSO4是一种难溶于水的强电解质;③冰醋酸、纯碱、小苏打分别属于酸、碱、盐;④太阳能、氢能和海洋能都属于新能源;⑤置换反应都属于离子反应.其中正确的是( )| A. | ①②⑤ | B. | ①②④ | C. | ②③④ | D. | ③④⑤ |
分析 ①由不同种分子构成的物质为混合物;
②大多数盐均属于强电解质;
③纯碱叫碱不是碱,属于盐类;
④太阳能、氢能和海洋能都属于新能源;
⑤有的置换反应属于离子反应,有的不是.
解答 解:①由不同种分子构成的物质为混合物,Fe(OH)3胶体和CuSO4溶液都是混合物的两大分支,故①正确;
②BaSO4是一种难溶于水的盐类物质,属于强电解质,故②正确;
③纯碱是碳酸钠的俗称,叫碱不是碱,属于盐类,故③错误;
④太阳能、氢能和海洋能都属于新能源,故④正确;
⑤有的置换反应属于离子反应,有的不是,如C和CuO的反应,故⑤错误.故选B.
点评 本题是一道有关物质分类的题目,难度不大,可以根据所学的知识进行回答.

练习册系列答案
相关题目
15.配制250mL 2mol/L的稀盐酸,需要12.5mol/L的浓盐酸的体积为( )
| A. | 20mL | B. | 40mL | C. | 60mL | D. | 80mL |
2. 铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
(一)高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
(1)该反应的平衡常数表达式K=$\frac{c(C{O}_{2})}{c(CO)}$;△H<0(填“>”、“<”或“=”).
(2)欲提高上述反应中CO的平衡转化率,可采取的措施是B.
A.提高反应温度 B.移出部分CO2
C.加入合适的催化剂 D.减小容器的容积
(3)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正>υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)=0.008 mol/(L•min).
(二)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.
(4)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,其中反应的氧化剂是KClO;生成0.5mol K2FeO4转移电子的物质的量是1.5mol.
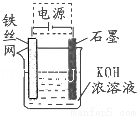
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图所示.电解过程中阳极的电极反应式为Fe+8OH--6e-═FeO42-+4H2O.
 铁及其化合物在生产、生活中有广泛应用.请回答下列问题:
铁及其化合物在生产、生活中有广泛应用.请回答下列问题:(一)高炉炼铁过程中发生的主要反应为:$\frac{1}{3}$Fe2O3(s)+CO(g)?$\frac{2}{3}$Fe(s)+CO2(g)
已知该反应在不同温度下的平衡常数如下:
| 温度/℃ | 1000 | 1115 | 1300 |
| 平衡常数 | 4.0 | 3.7 | 3.5 |
(2)欲提高上述反应中CO的平衡转化率,可采取的措施是B.
A.提高反应温度 B.移出部分CO2
C.加入合适的催化剂 D.减小容器的容积
(3)在一个容积为10L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时υ正>υ逆(填“>”、“<”或“=”).经过10min,在1000℃达到平衡,则该时间范围内反应的平均反应速率υ(CO2)=0.008 mol/(L•min).
(二)高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂.
(4)一定条件下Fe(OH)3与KClO在KOH溶液中反应可制得K2FeO4,其中反应的氧化剂是KClO;生成0.5mol K2FeO4转移电子的物质的量是1.5mol.
(5)从环境保护的角度看,制备K2FeO4较好的方法为电解法,其装置如图所示.电解过程中阳极的电极反应式为Fe+8OH--6e-═FeO42-+4H2O.
19.在一定温度下,可逆反应:A(g)+3B(g)?2C(g)达到化学平衡的标志是( )
| A. | C的生成速率与C的分解速率相等 | |
| B. | A、B、C的分子数之比是1:3:2 | |
| C. | 单位时间内生成n molA,同时生成3n mol B | |
| D. | A、B、C的浓度相等 |
20.下列说法正确的是( )
| A. | 碳碳间以单键结合,碳原子剩余价键全部与氢原子结合的烃一定是饱和链烃 | |
| B. | 分子组成符合CnH2n+2的烃一定是烷烃 | |
| C. | 烷烃分子中所有的碳原子均在同一条直线上 | |
| D. | 甲烷和异丁烷互为同系物 |
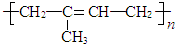 .
.