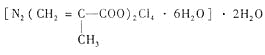��Ŀ����
����Ŀ���ش������⣺
��1��C��N��O����Ԫ�صĵ�һ�������ɴ�С��˳����__________________��
��2��C��Si��N�ĵ縺���ɴ�С��˳����__________________��
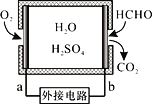
��3��������ˮ��Һ�д��ڵ������_________�֡�
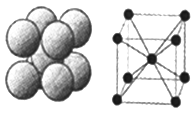
��4�����������仯�����ںϽ�����Լ������ȷ���Ӧ�ù㷺��Ni�Ļ�̬ԭ����________��������ͬ�ĵ��ӡ��ܶ�����л�����Ni���¿���H2�����ӳɷ�Ӧ������CH2=CH2����HC��CH����![]() ����HCHO������̼ԭ�Ӳ�ȡsp2�ӻ��ķ�����__________(�����ʱ��)��HCHO���ӵ����幹��Ϊ______________��
����HCHO������̼ԭ�Ӳ�ȡsp2�ӻ��ķ�����__________(�����ʱ��)��HCHO���ӵ����幹��Ϊ______________��
���𰸡���1�� N>O>C��2�֣� ��2��N>C>Si��2�֣�
��3��4��2�֣�����4��7��1�֣����٢ۢ���2�֣���
ƽ�������Σ����������Σ���1�֣�
�����������⣨1��һ�������ͬһ���ڵ�Ԫ�أ�ԭ������Խ��Ԫ�صķǽ�����Խǿ��Ԫ�صĵ�һ������Խ��������Nԭ���������Ӵ��ڰ�������ȶ�״̬�����һ�����ܱ�O��������C��N��O����Ԫ�صĵ�һ�������ɴ�С��˳����N>O>C����2��Ԫ�صķǽ�����N>C>Si��Ԫ�صķǽ�����Խǿ����縺��Խ������C��Si��N�ĵ縺���ɴ�С��˳����N>C>Si����3��������ˮ��Һ�д��ڵ������HF����֮��������ˮ����֮��������ˮ���ӵ�Hԭ����HF���ӵ�Fԭ��֮��������HF���ӵ�Hԭ����ˮ���ӵ�Oԭ��֮���γɵ��������˹���4���������4��Ni��28��Ԫ�أ���������Ų�ʽ��1s22s22p63s23p63d84s2��ͬһ�Dz�ĵ���������ͬ������Ni�Ļ�̬ԭ����7��������ͬ�ĵ��ӡ�����CH2=CH2��̼ԭ����sp2�ӻ�����HC��CH��sp�ӻ�����![]() ����̼ԭ����sp2�ӻ�����HCHO��̼ԭ����sp2�ӻ���������̼ԭ�Ӳ�ȡsp2�ӻ��ķ������٢ۢ���HCHO���ӵ����幹��Ϊƽ�������Σ����������Σ���
����̼ԭ����sp2�ӻ�����HCHO��̼ԭ����sp2�ӻ���������̼ԭ�Ӳ�ȡsp2�ӻ��ķ������٢ۢ���HCHO���ӵ����幹��Ϊƽ�������Σ����������Σ���

 ��ս�п�����ϵ�д�
��ս�п�����ϵ�д�