题目内容
12.下列有关实验叙述错误的是( )| A. | 实验室可用硫酸铜溶液除去乙炔中的H2S等杂质气体 | |
| B. | 苯和溴水在溴化铁溶液催化作用下发生取代反应生成溴苯 | |
| C. | 只用溴水就可以将苯、四氯化碳、酒精、氢氧化钠溶液这四种物质区别开 | |
| D. | 将铜丝在酒精灯上加热变黑后,立即伸入无水乙醇中,铜丝恢复成原来的红色 |
分析 A.硫酸铜与硫化氢反应生成CuS沉淀可除杂,而乙炔不反应;
B.苯和溴水不反应;
C.苯、四氯化碳、酒精、氢氧化钠溶液分别与溴水混合的现象为:分层后有机层在上层、分层后有机层在下层、不分层、溶液为无色且不分层;
D.铜丝在酒精灯上加热变黑后生成CuO,立即伸入无水乙醇中,铜丝恢复成原来的红色,可知CuO被乙醇还原.
解答 解:A.硫酸铜与硫化氢反应生成CuS沉淀可除杂,而乙炔不反应,则可用硫酸铜溶液除去乙炔中的H2S等杂质气体,故A正确;
B.苯和溴水不反应,不能制备溴苯,应选苯和液溴在溴化铁溶液催化作用下发生取代反应生成溴苯,故B错误;
C.苯、四氯化碳、酒精、氢氧化钠溶液分别与溴水混合的现象为:分层后有机层在上层、分层后有机层在下层、不分层、溶液为无色且不分层,现象不同可鉴别,故C正确;
D.铜丝在酒精灯上加热,Cu被氧化生成CuO,则变黑,立即伸入无水乙醇中,CuO被乙醇还原,生成Cu,则铜丝恢复成原来的红色,故D正确;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及有机物的制备、性质及混合物分离提纯、物质鉴别等,把握物质的性质、反应原理、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
2.已知某原子的结构示意图为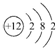 ,下列说法正确的是( )
,下列说法正确的是( )
 ,下列说法正确的是( )
,下列说法正确的是( )| A. | 该元素位于第3周期第ⅡA族 | B. | 该元素位于第2周期第Ⅷ族 | ||
| C. | 该元素位于第2周期第ⅡA族 | D. | 该元素位于第4周期第ⅡB族 |
20.常温下,某无色溶液能与铝反应放出氢气,该溶液中一定能大量存在的离子组是( )
| A. | Na+、K+、MnO4-、SO42- | B. | Mg2+、NH4+、SO42-、Cl- | ||
| C. | Na+、Cl-、K+、SO42- | D. | Na+、K+、CO32-、NO3- |
4.下列事实不能用平衡移动原理解释的是( )
| A. | 用排饱和食盐水法收集Cl2 | |
| B. | 二氧化硫转化为三氧化硫时增加空气的量以提高二氧化硫的转化率 | |
| C. | 加入催化剂可以提高原料转化率,生成更多产物 | |
| D. | 分别用等体积的蒸馏水和0.01mol/L的硫酸洗涤BaSO4沉淀,用水洗涤造成BaSO4的损失量大于用稀硫酸洗涤的损失量 |
1.下列关于金属钠性质的叙述中,正确的是( )
| A. | 钠是密度小、硬度大、熔点高的银白色金属 | |
| B. | 钠在纯净的氧气中充分燃烧,生成白色固体Na2O | |
| C. | 将金属钠放入CuSO4溶液中,可观察到大量红色的铜析出 | |
| D. | 将金属钠放入水中立即熔化成小球,说明金属钠熔点低,且反应放出热量 |
2.寻找清洁能源一直是化学家努力的方向,下列关于能源的说法错误的是( )
| A. | 氢气热值高,其燃烧产物是水,是一种理想的清洁燃料 | |
| B. | 利用太阳能等清洁能源代替化石燃料,有利于节约资源,保护环境 | |
| C. | 煤的气化技术在一定程度上实现了煤的高效、清洁利用 | |
| D. | 石油作为重要的可再生能源应该被尽量地利用 |
 ②CH3CH2CH(CH3)CH3 ③CH4 ④
②CH3CH2CH(CH3)CH3 ③CH4 ④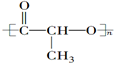 ⑤
⑤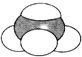 ⑥
⑥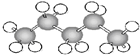 ⑦
⑦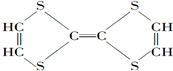

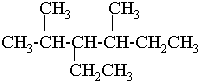
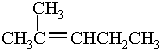 .
.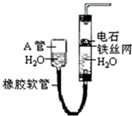 由图中的实验装置可用于制取乙炔,请回答
由图中的实验装置可用于制取乙炔,请回答