题目内容
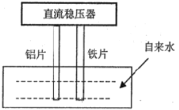
【题目】Ⅰ、研究性学习小组进行SO2的制备及性质探究实验,装置如图(a为活塞,加热及固定装置已略去)。

(1)连接仪器、___、加药品后,打开 a,然后滴入浓硫酸,加热;
(2)铜与浓硫酸反应制备 SO2的化学方程式是___;
(3)品红溶液中的实验现象是___;
(4)从高锰酸钾溶液中观察到的现象说明 SO2具有___性。
Ⅱ、上述实验中 NaOH 溶液用于吸收剩余的 SO2 生成 Na2SO3,Na2SO3是抗氧剂。向烧碱和Na2SO3混合溶液中加入少许溴水,振荡后溶液变为无色。
(1)写出在碱性溶液中Br2氧化Na2SO3的离子方程式___
(2)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO42-和Br-的实验报告。___
限选试剂:2mol·L-1HCl;1mol·L-1H2SO4;lmol·L-1BaCl2;lmol·L-1Ba(NO3)2;0.1mol·L-1AgNO3;CCl4;新制氯水。
编号 | 实验操作 | 预期现象和结论 |
步骤① | 取少量待测液加入试管中,加入过量的2mol·L-1盐酸,再滴加 | 有 生成,证明待测液中SO42- |
步骤② | 取出步骤①中适量上层清液于试管中,加入适量氯水,再加入 ,振荡,静置。 | 下层液体呈 ,证明待测液中含Br-。 |
【答案】检查装置气密性 Cu +2H2SO4(浓)![]() CuSO4+SO2↑+2H2O 品红溶液红色褪去变为无色 还原性 SO32-+Br2+2OH-=H2O+SO42-+2Br-
CuSO4+SO2↑+2H2O 品红溶液红色褪去变为无色 还原性 SO32-+Br2+2OH-=H2O+SO42-+2Br-
编号 | 实验操作 | 预期现象和结论 |
步骤① | lmol·L-1BaCl2溶液 | 有白色沉沉淀生成 |
步骤② | 四氯化碳 | 橙黄色 |
【解析】
Ⅰ、(1)依据装置制备气体验证气体性质分析步骤;
(2)铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水;
(3)依据二氧化硫的漂白性解释;
(4)二氧化硫通入高锰酸钾溶液中发生氧化还原反应使高锰酸钾溶液褪色;
II、(1) Na2SO3和溴发生氧化还原反应;
(2)检验SO42-,可用硝酸酸化的BaCl2;检验Br2,可用氯水,加入四氯化碳后,根据四氯化碳层的颜色进行判断。
Ⅰ、(1)装置是制备气体的反应,连接好装置需要检验装置的气密性,再加入试剂发生反应;
故答案为检验装置气密性;
(2)铜和浓硫酸加热反应生成硫酸铜、二氧化硫和水,反应的化学方程式:Cu +2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
故答案为Cu +2H2SO4(浓)![]() CuSO4+SO2↑+2H2O;
CuSO4+SO2↑+2H2O;
(3)二氧化硫具有漂白性,能使品红溶液红色褪去;
故答案为品红溶液红色褪去变为无色;
(4)二氧化硫具有还原性通入高锰酸钾溶液被氧化为硫酸,高锰酸钾溶液紫红色褪去变化为无色;
故答案为还原性;
II、(1)向烧碱和Na2SO3混合溶液中加入少许溴水,振荡后溶液变为无色,说明亚硫酸根离子被溴单质氧化为硫酸跟,依据得失电子守恒和原子守恒配平写出离子方程式为:SO32-+Br2+2OH-=H2O+SO42-+2Br-;
故答案为SO32-+Br2+2OH-=H2O+SO42-+2Br-;
(2)、检验SO42-可取少量待测液加入试管中,加入过量的2 mol/L盐酸,再滴加适量l mol/LBaCl2溶液;检验Br-,可取出步骤①中适量上层清液于试管中,加入适量氯水,再加入四氯化碳,振荡,静置后观察颜色,如若下层液体呈橙红色,证明待测液中含Br-;
故答案为
编号 | 实验操作 | 预期现象和结论 |
步骤① | lmol·L-1BaCl2溶液 | 有白色沉沉淀生成 |
步骤② | 四氯化碳 | 橙黄色 |
。