题目内容
【题目】1934年,居里夫妇![]() 粒子(4He)轰击27Al得到一种自然界中不存在的磷元素的一种核素(
粒子(4He)轰击27Al得到一种自然界中不存在的磷元素的一种核素(![]() ):
):![]() +
+![]()
![]()
![]() +
+![]() ,开创了人造核素的先河。
,开创了人造核素的先河。
(1)下列有关说法正确的有______(填序号)。
A. ![]() 的质子数是27 B.
的质子数是27 B. ![]() 是一种电中性粒子
是一种电中性粒子
C. ![]() 和
和![]() 互为同位素 D. P元素的相对原子质量为30
互为同位素 D. P元素的相对原子质量为30
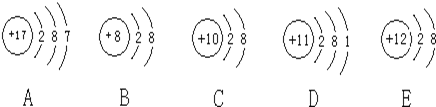
(2)元素的化学性质主要取决于______(填序号)。
A. 原子最外层电子数 B. 原子核内中子数
C. 原子核内质子数 D. 原子质量数
(3)不同种元素的本质区别是______(填序号)。
A. 原子的质子数不同 B. 原子的中子教不同
C. 原子的最外层电子数不同 D. 原子的质量数不同
【答案】BC A A
【解析】
(1)根据微粒符号表示中各个角标的含义,及同位素的概念和质量数与元素相对原子质量的关系、元素相对原子质量与同位素原子质量数关系分析;
(2)根据物质在发生化学反应时通常是原子的最外层电子发生变化分析;
(3)根据元素的含义分析判断。
(1)A. ![]() 的质子数是13,质量数是27,A错误;
的质子数是13,质量数是27,A错误;
B. ![]() 表示质子数是0,中子数是1的微粒,即表示中子,中子是一种电中性粒子,B正确;
表示质子数是0,中子数是1的微粒,即表示中子,中子是一种电中性粒子,B正确;
C. ![]() 和
和![]() 的质子数都是2,中子数分别是2、1,可见两种微粒质子数相同,中子数不同,因此二者互为同位素,C正确;
的质子数都是2,中子数分别是2、1,可见两种微粒质子数相同,中子数不同,因此二者互为同位素,C正确;
D. ![]() 的质量数是30,但P元素有几种同位素原子,各种同位素原子的原子个数比未知,因此不能确定P元素的相对原子质量,D错误;
的质量数是30,但P元素有几种同位素原子,各种同位素原子的原子个数比未知,因此不能确定P元素的相对原子质量,D错误;
故合理选项是BC;
(2)物质在发生化学反应时,原子核不变,内层电子也不变,变化的通常是原子的最外层电子,所以元素的化学性质主要取决于原子核外最外层电子数,故合理选项是A;
(3)同种元素的原子,质子数相同;不同元素的原子,质子数不同,可见判断元素是否属于不同种元素,本质区别是看原子核内质子数的多少,通常把具有相同的核电荷数即质子数的同一类原子总称为元素,故合理选项是A。

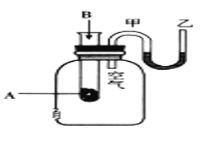
【题目】Ⅰ、研究性学习小组进行SO2的制备及性质探究实验,装置如图(a为活塞,加热及固定装置已略去)。

(1)连接仪器、___、加药品后,打开 a,然后滴入浓硫酸,加热;
(2)铜与浓硫酸反应制备 SO2的化学方程式是___;
(3)品红溶液中的实验现象是___;
(4)从高锰酸钾溶液中观察到的现象说明 SO2具有___性。
Ⅱ、上述实验中 NaOH 溶液用于吸收剩余的 SO2 生成 Na2SO3,Na2SO3是抗氧剂。向烧碱和Na2SO3混合溶液中加入少许溴水,振荡后溶液变为无色。
(1)写出在碱性溶液中Br2氧化Na2SO3的离子方程式___
(2)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO42-和Br-的实验报告。___
限选试剂:2mol·L-1HCl;1mol·L-1H2SO4;lmol·L-1BaCl2;lmol·L-1Ba(NO3)2;0.1mol·L-1AgNO3;CCl4;新制氯水。
编号 | 实验操作 | 预期现象和结论 |
步骤① | 取少量待测液加入试管中,加入过量的2mol·L-1盐酸,再滴加 | 有 生成,证明待测液中SO42- |
步骤② | 取出步骤①中适量上层清液于试管中,加入适量氯水,再加入 ,振荡,静置。 | 下层液体呈 ,证明待测液中含Br-。 |