题目内容
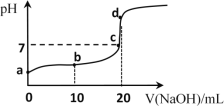
【题目】在恒压、NO和O2的起始浓度一定的条件下,催化反应相同时间,测得不同温度下NO转化为NO2的转化率如图中实线所示(图中虚线表示相同条件下NO的平衡转化率随温度的变化)。下列说法正确的是( )
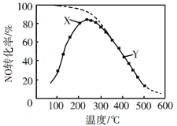
A.反应2NO(g)+O2(g)=2NO2(g)的ΔH>0
B.图中X点所示条件下,延长反应时间能提高NO转化率
C.图中Y点所示条件下,增加O2的浓度不能提高NO转化率
D.380℃下,c起始(O2)=5.0×104 mol·L1,NO平衡转化率为50%,则平衡常数K<2000
【答案】B
【解析】
A. 根据图像可知,升高温度,NO的转化率逐渐降低,说明升高温度,平衡逆向移动;
B. X点时反应没有达到平衡状态,平衡正向移动;
C. Y点时反应为平衡状态,增大反应物的浓度,平衡正向移动;
D. 利用三段法结合平衡常数进行计算。
A. 根据图像可知,升高温度,NO的转化率逐渐降低,说明平衡逆向移动,正向反应放热,则ΔH<0,A项错误;
B. X点时反应没有达到平衡状态,平衡正向移动,延长时间能提高NO的转化率,B项正确;
C. Y点时反应为平衡状态,增大反应物的浓度,平衡正向移动,NO的转化率增大,C项错误;
D.设起始时NO的浓度为xmol/L,NO平衡转化率为50%,则NO转化了0.5xmol/L,
2NO(g) + O2(g) = 2NO2(g)
始(mol/L) x 5.0×104 0
转(mol/L) 0.5x 0.25x 0.5x
平(mol/L) 0.5x 5.0×104-0.25x 0.5x
平衡常数K=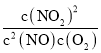 =
=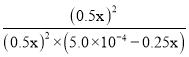 >2000,D项错误;
>2000,D项错误;
答案选B。

 名校课堂系列答案
名校课堂系列答案【题目】在3种不同条件下,分别向容积为2L的恒容密闭容器中充入2molA和1molB,发生反应:2A(g)+B(g)![]() 2D(g)△H=QkJ/mol。相关条件和数据见下表:
2D(g)△H=QkJ/mol。相关条件和数据见下表:
实验编号 | 实验I | 实验II | 实验III |
反应温度/℃ | 700 | 700 | 750 |
达平衡时间/min | 40 | 50 | 30 |
n(D)平衡/mol | 1.5 | 1.5 | 1 |
化学平衡常数 | K1 | K2 | K3 |
下列说法正确的是
A. 升高温度能加快反应速率的原理是降低了反应的活化能,使活化分子百分数提高
B. 实验III达平衡后,保持其他条件不变,再向容器中通入1molA和1molD,平衡不移动
C. 实验III达平衡后容器内的压强是实验1的9/10倍
D. K3>K2>K1