题目内容
【题目】中国古代文献中记载了大量古代化学的研究成果,《本草纲目》中记载:“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”,反应原理为:S+2KNO3+3C===K2S+N2↑+3CO2↑。
(1)氮原子的价层电子排布图为___________,烟花燃放过程中,钾元素中的电子跃迁的方式是___________,K、S、N、O四种元素第一电离能由大到小的顺序为___________。上述反应涉及的元素中电负性最大的是___________(填元素符号)。
(2)碳元素除可形成常见的氧化物CO、CO2外,还可形成C2O3(结构式为![]() )。C2O3与水反应可生成草酸(HOOC—COOH)。
)。C2O3与水反应可生成草酸(HOOC—COOH)。
①C2O3中碳原子的杂化轨道类型为___________,CO2分子的立体构型为___________。
②草酸与正丁酸(CH3CH2CH2COOH)的相对分子质量相差2,二者的熔点分别为101℃、-7.9℃,导致这种差异的最主要原因可能是______________________。
③CO分子中π键与σ键个数比为___________。
(3)超氧化钾的晶胞结构图如下:
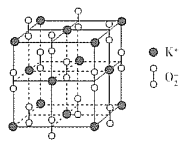
则与K+等距离且最近的K+个数为___________,若晶胞参数为dpm,则该超氧化物的密度为___________g·cm-3(用含d、NA的代数式表示,设NA表示阿伏加德罗常数的值)。
【答案】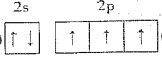 由高能量状态跃迁到低能量状态 N>O>S>K O sp2 直线型 草酸分子间能形成更多氢键 2:1 12
由高能量状态跃迁到低能量状态 N>O>S>K O sp2 直线型 草酸分子间能形成更多氢键 2:1 12 ![]()
【解析】
根据核外电子排布特点及非金属性强弱比较第一电离能大小;根据等电子体结构及杂化轨道理论分析分子的空间结构;根据晶胞的结构计算晶胞的密度。
(1)N原子价电子数为5,其电子排布图为 ;焰色反应属于发射光谱,故电子是由高能量状态跃迁到低能量状态,由第一电离能递变规律及N原子的2p能级处于半充满状态得第一电离能的大小顺序为N>O>S>K;上述反应涉及的元素中氧元素的非金属性最强,故电负性最大,
;焰色反应属于发射光谱,故电子是由高能量状态跃迁到低能量状态,由第一电离能递变规律及N原子的2p能级处于半充满状态得第一电离能的大小顺序为N>O>S>K;上述反应涉及的元素中氧元素的非金属性最强,故电负性最大,
故答案为:; ;由高能量状态跃迁到低能量状态;N>O>S>K;O;
;由高能量状态跃迁到低能量状态;N>O>S>K;O;
(2)①C2O3中碳原子形成3个σ键、为sp2杂化;CO2中C原子采取sp杂化,立体构型为直线型;
②草酸分子中有2个O-H键,丁酸分子中只含有一个O-H键,故草酸分子间形成的氢键数目比丁酸分子间形成的氢键数目多,因此其沸点比较高;
③CO与N2互为等电子体,结构相似,故π键与σ键个数比为2:1;
故答案为:sp2;直线型;草酸分子间能形成更多氢键;2:1;
(3)由晶胞图知,同一平面内与K+距离相等且最近的K+有4个,通过某一个K+且相互垂直的平面有3个,故共有12个K+符合条件;由均摊原理知每个晶胞中含有4个KO2,质量为4/NA×71g,晶胞的体积为d3×10-30cm3,故密度为:![]() g/cm3,
g/cm3,
故答案为:12;![]() 。
。

 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案【题目】自然界井不缺少“镁”,缺少的是发现“镁”的眼晴。海水中镁的绝对含量高但相对浓度却小[c(Mg2+)约为0.054mo1L﹣1]。工业上常从海水中提镁,其生产过程的讨论方案如图所示:
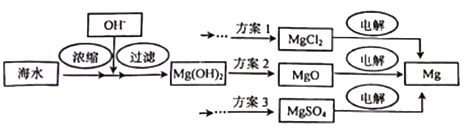
(1)要实现对海水中镁元素的富集,一般采取______(填编号)。①直接往海水中加入沉淀剂;②利用晒盐后的苦卤水,向其中加入沉淀剂;③先加热蒸发海水,再加入沉淀剂
(2)根据表中4种试剂的市场价格数据,选择_____做沉淀剂最合理,如果“提镁”工厂就建在海边,____是生产这种试剂的最好原料。
试剂 | NaOH | KOH | Ca(OH)2 | Ba(OH)2 |
价格(元/吨) | 3300 | 9500 | 580 | 3500 |
(3)根据下表中3种电解质的熔点数据,上图方案中,方案______最优,此方案采取电解熔融态电解质而不是电解其水溶液,原因是______;电解的化学方程式为_____。
电解质 | MgCl2 | MgO | MgSO4 |
熔点/℃ | 714 | 2800 | 1327 |
(4)电解所得的镁蒸气冷却后即为固体镁,冷却镁蒸气可以选择_______氛围。
A、N2 B、CO2 C.Ar D.空气