题目内容
9.下列说法中,正确的是( )| A. | 1 mol H2SO4与1 molBa(OH)2反应生成H2O时放出的热叫做中和热 | |
| B. | △H>0 kJ•mol-1表示放热反应,△H<0 kJ•mol-1表示吸热反应 | |
| C. | 热化学方程式中的化学计量数表示物质的量,可以是分数 | |
| D. | 1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
分析 A、中和热的本质是在稀溶液中,1mol氢离子与1mol氢氧根反应,生成1mol水放出的热量.
B、焓变△H>0表示吸热反应,△H<0,表示放热反应.
C、热化学方程式中的化学计量既表示物质的量.
D、在25℃,101 kPa时,1 mol可燃物完全燃烧生成稳定的化合物时所放出的热量,叫做该物质的燃烧热.
解答 解:A、1 mol H2SO4与1 molBa(OH)2反应生成水的物质的量不是1mol,且有钡离子与硫酸根反应生成硫酸钡沉淀,也有热量放出,故A错误;
B、焓变△H>0表示吸热反应,△H<0,表示放热反应,故B错误;
C、热化学方程式中的化学计量既表示物质的量也可以表示个数,所以可以是分数,故C正确;
D、应在25℃,101 kPa,且生成的水应为液态,故D错误.
故选:C.
点评 本题考查了燃烧热、中和热、焓变概念的理解和应用,热化学方程式的含义理解分析,题目较简单.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
19.常温下,向0.25mol•L-1的硫酸溶液中逐滴加入物质的量浓度相同的氢氧化钡溶液,生成沉淀的量与加入氢氧化钡溶液的体积关系如图所示,a、b、c、d分别表示实验不同时刻的溶液,下列有关说法中正确的是( )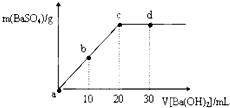

| A. | 硫酸溶液的体积为30 mL | |
| B. | b时刻溶液中SO42-的浓度约为0.125 mol•L-1 | |
| C. | d时刻溶液的pH约为13 | |
| D. | 溶液的导电能力:c<d=b<a |
17.下列物质属于纯净物的是( )
| A. | 葡萄糖 | B. | 聚乙烯 | C. | 医用酒精 | D. | 油脂 |
4.据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍.其电池反应为:2CH3OH+3O2+4OH-$?_{充电}^{放电}$2CO32-+6H2O,则下列说法错误的是( )
| A. | 放电时负极的电极反应为:CH3OH-6e-+8OH-═CO${\;}_{3}^{2-}$+6H2O | |
| B. | 充电时电解质溶液的pH逐渐增大 | |
| C. | 放电时CH3OH参与反应的电极为正极 | |
| D. | 充电时每生成1 mol CH3OH转移6 mol电子 |
14.18O是一种示踪原子,用来探究反应历程.在密闭容器中加入CO和H218O发生反应CO+H218O═CO2+H2,一段时间后达到平衡,18O存在于下列哪些微粒中( )
| A. | 只存在于CO2中 | B. | 只存在于CO中 | ||
| C. | 存在于CO2和H2O中 | D. | 存在于CO、H2O和CO2中 |
1.乙烯与高锰酸钾反应会放出CO2,下列操作中既可以用来鉴别乙烯和乙烷,又可以用来除去乙烷中混有的少量乙烯的操作方法是( )
| A. | 混合气通过盛有水的洗气瓶 | |
| B. | 通过装有过量溴水的洗气瓶 | |
| C. | 混合气通过装有酸性高锰酸钾溶液的洗气瓶 | |
| D. | 混合气与过量氢气混合 |
18.下列说法中不正确的是( )
| A. | 用完的电池不可以随意地丢弃 | |
| B. | 增加炼铁高炉的高度不能降低尾气中CO的含量 | |
| C. | 无论加入正催化剂还是加入负催化剂都能大大提高化学反应速率 | |
| D. | 把煤粉碎后再燃烧可以提高煤的燃烧效率 |
19.在体积恒定的密闭容器中,不能说明可逆反应2A(g)?3B(g)+2C(g)已达到平衡状态的是(一定温度下)( )
| A. | 密闭容器中混和气体的密度不再发生变化 | |
| B. | 混和气体的平均相对分子质量不再发生变化 | |
| C. | 单位时间内生成3mol B的同时有2mol A生成 | |
| D. | A的生成速率与A的分解速率相等 |