题目内容
19.在体积恒定的密闭容器中,不能说明可逆反应2A(g)?3B(g)+2C(g)已达到平衡状态的是(一定温度下)( )| A. | 密闭容器中混和气体的密度不再发生变化 | |
| B. | 混和气体的平均相对分子质量不再发生变化 | |
| C. | 单位时间内生成3mol B的同时有2mol A生成 | |
| D. | A的生成速率与A的分解速率相等 |
分析 当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的物理量不变,据此分析解答.
解答 解:A.反应前后气体质量不变、容器体积不变,所以密度始终不变,所以不能根据密度判断平衡状态,故A选;
B.该反应前后气体物质的量之和增大,气体质量不变,所以气体平均分子质量随着反应进行而减小,当混合气体平均相对分子质量不变时,正逆反应速率相等该反应达到平衡状态,故B不选;
C.无论反应是否达到平衡状态,都存在单位时间内生成3mol B的同时由2mol A生成,所以不能据此判断平衡状态,故C选;
D.A的生成速率与A的分解速率相等,则正逆反应速率相等,该反应达到平衡状态,故D不选;
故选AC.
点评 本题考查化学平衡状态判断,为高频考点,只有前后前后改变的物理量不变时可逆反应就达到平衡状态,易错选项是A.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
9.下列说法中,正确的是( )
| A. | 1 mol H2SO4与1 molBa(OH)2反应生成H2O时放出的热叫做中和热 | |
| B. | △H>0 kJ•mol-1表示放热反应,△H<0 kJ•mol-1表示吸热反应 | |
| C. | 热化学方程式中的化学计量数表示物质的量,可以是分数 | |
| D. | 1 mol H2与0.5 mol O2反应放出的热就是H2的燃烧热 |
10.能够证明SO2中含有CO2的方法是将气体( )
| A. | 通入澄清石灰水 | |
| B. | 先通入酸性KMnO4溶液,再通入石灰水 | |
| C. | 通入品红溶液 | |
| D. | 先通入饱和NaHCO3溶液,在通入石灰水 |
7.下列属于取代反应的是( )
| A. | 用漫射散光照射甲烷与氯气的混合气体 | |
| B. | 乙烯通入溴水中 | |
| C. | 在镍做催化剂的条件下,苯与氢气反应 | |
| D. | 乙醇与酸性高锰酸钾溶液反应 |
14.将5.6 L(标准状况)乙烯和甲烷的混合气体通入足量溴水中,充分反应后,溴水的质量增加了2.8 g.原混合气体中乙烯与甲烷的质量比是( )
| A. | 2:1 | B. | 2:3 | C. | 7:6 | D. | 7:3 |
4.按酸碱质子理论,下列粒子既可看作酸又可看作碱的是( )
| A. | CH3COO- | B. | NH4+ | C. | OH- | D. | HCO3- |
11.下列装置或操作不能达到实验目的是( )
| A. | 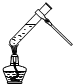 葡萄糖的银镜反应 | B. | 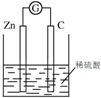 形成原电池 | ||
| C. | 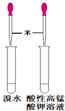 检验苯中有无碳碳双键 | D. | 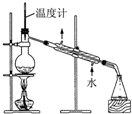 石油的分馏 |
8.为验证蔗糖能水解,且水解产物有还原性,可能有以下实验步骤:(1)加入稀硫酸;(2)加入几滴CuSO4溶液;(3)加热;(4)加入蒸馏水;(5)加入烧碱溶液至中性;(6)加入新制Cu(OH)2.最佳顺序是( )
| A. | (4)(1)(3)(6)(3) | B. | (4)(3)(1)(6)(5)(3) | C. | (1)(3)(2)(6)(3) | D. | (4)(1)(3)(5)(6)(3) |
9.NA表示阿伏伽德罗常数,下列叙述正确的是( )
| A. | 125g CuSO4•5H2O晶体中含有Cu2+离子数一定小于0.5NA | |
| B. | 常温下,pH=3的醋酸溶液中,醋酸分子的数目一定大于10-3NA | |
| C. | 由S6、S7、S8组成的硫蒸气6.4g,其中所含硫原子数一定为0.2NA | |
| D. | 3.6g C与3.36L O2一定条件下恰好完全反应,生成CO分子数一定为0.3NA |