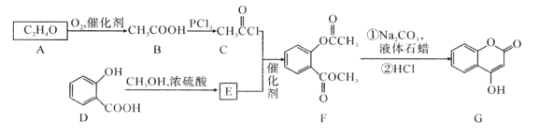
题目内容
【题目】pc类似pH,是指极稀溶液中溶质物质的量浓度的常用对数负值。如某溶液溶质的浓度为1×10-3mol/L,则该溶液溶质的pc=3。下列说法正确的是
A.25°C时,0.01mol/LNa2S水溶液中,pc(H+)+pc(OH-)=14
B.用0.01mol/L的NaOH溶液滴定某浓度的盐酸,滴定过程中pc(OH-)逐渐增大
C.某温度下,弱酸HB的Ka=1×10-5mol/L,则该溶液中pc(H+)+pc(B-)=l0
D.向0.0lmol/L的Ca(HCO3)2溶液中逐渐滴加烧碱溶液,滴加过程中pc(Ca2+)逐渐减小
【答案】A
【解析】
A.25°C时,![]() ,所以0.01mol/LNa2S水溶液中,pc(H+)+pc(OH-)=14,故A正确;
,所以0.01mol/LNa2S水溶液中,pc(H+)+pc(OH-)=14,故A正确;
B.用0.01mol/L的NaOH溶液滴定某浓度的盐酸,滴定过程中c(OH-)逐渐增大,pc(OH-)逐渐减小,故B错误;
C.某温度下,弱酸HB的Ka=1×10-5mol/L,由于不知HB的浓度,则该溶液中pc(H+)+pc(B-)的值不确定,故C错误;
D.向0.0lmol/L的Ca(HCO3)2溶液中逐渐滴加烧碱溶液,反应生成碳酸钙沉淀,钙离子浓度降低,滴加过程中pc(Ca2+)逐渐增大,故D错误;
选A。

 名校课堂系列答案
名校课堂系列答案【题目】微型实验具有装置小巧、节约药品、操作简便、现象明显、安全可靠、减少污染等优点,下图是某同学设计的实验室制取Cl2并探究其化学性质的微型装置(图中夹持装置均略去)。
查阅资料:氯气的氧化性大于HIO3。
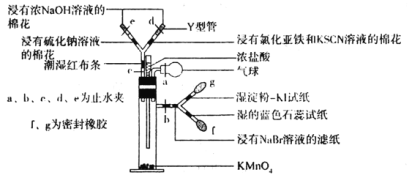
回答下列问题:
(1)实验室中可代替图中添加浓盐酸的仪器名称是___________。
(2)加入浓盐酸后试管内发生反应的化学方程式是__________________________________。
(3)探究氯气的化学性质,将实验现象填写在下表对应的空格里:___________
操作步骤 | 实验现象 |
缓慢加入浓盐酸,打开c、d、e,使产生的氯气缓慢充入Y试管 | |
关闭c打开b,使氯气缓慢进入Y管中 |
(4)实验中发现若氯气的通入量过多,淀粉碘化钾试纸会逐渐变为无色,可能的原因是__________________________________________________。
(5)此装置___________(填“能”或“不能”)证明氧化性顺序Cl2>Br2>I2,原因是___________,实验完毕后,关闭止水夹b,打开a、c,挤压气球,目的是__________________________。
【题目】(1)通常人们把拆开1mol某化学键所吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可用于估算化学反应的反应热(△H)。
化学键 | Si—O | Si—Cl | H—H | H—Cl | Si—Si | Si—C |
键能/kJ·mol—1 | 460 | 360 | 436 | 431 | 176 | 347 |
请回答下列问题:
①比较下列两组物质的熔点高低(填“>”或“<”=)
SiC_____________Si;SiCl4_____________SiO2
②工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g)该反应的反应热△H=_____________kJ/mol.
Si(s)+4HCl(g)该反应的反应热△H=_____________kJ/mol.
(2)已知化合物Na2O的晶胞如图。
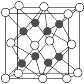
①其中O2-离子的配位数为________,
②该化合物与MgO相比,熔点较高的是________。(填化学式)
③已知该化合物的晶胞边长为apm,则该化合物的密度为___g·cm-3(只要求列出算式,不必计算出数值,阿伏加德罗常数的数值为NA)。