题目内容
8.工业上常将废旧铁屑(表面有油污)回收利用,用以制备绿矾(FeSO4•7H2O),绿矾、硫酸铵以相等物质的量混合可制得摩尔盐晶体,反应原理为:(NH4)2SO4+FeSO4+6H2O=(NH4)2SO4•FeSO4•6H2O↓.其流程可表示如图甲:
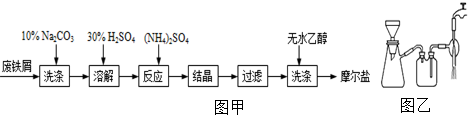
(1)洗涤中Na2CO3的主要作用是利用碳酸钠溶液呈碱性,除去铁表面的油污,请提出加快溶解的措施搅拌或加热(任答一点即可).
(2)结晶过程中要加热蒸发溶剂,浓缩结晶.应加热到加热到溶液表面出现晶膜时,停止加热.
(3)过滤是用如图乙装置进行,这种过滤跟普通过滤相比,除了过滤速度快外,还有一个优点是得到较干燥的沉淀.
(4)用无水乙醇洗涤的目的是除去水分,减少晶体溶解损失;容易干燥.
(5)产品中Fe2+的定量分析:制得的摩尔盐样品中往往含有极少量的Fe3+.为了测定摩尔盐产品中Fe2+的含量,一般采用在酸性条件下KMnO4标准液滴定的方法.称取4.0g的摩尔盐样品,溶于水,并加入适量稀硫酸.用0.2mol•L-1 KMnO4溶液滴定,当溶液中Fe2+ 全部被氧化时,消耗KMnO4溶液体积 10.00mL.
①写出滴定时反应的离子方程式5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O
②计算产品中Fe2+的质量分数(写出计算过程).
分析 制取摩尔盐晶体流程为:先利用碳酸钠溶液呈碱性,除去铁表面的油污,然后加稀硫酸溶解,铁与稀硫酸反应生成亚铁离子,加入硫酸铵发生(NH4)2 SO4+FeSO4+6H2O=(NH4)2SO4•FeSO4•6H2O↓,结晶过滤,摩尔盐易溶于水,难溶于有机溶剂,用酒精洗涤摩尔盐,得到摩尔盐晶体.
(1)Na2CO3溶液中CO32-水解使Na2CO3溶液呈碱性,油脂在碱性溶液中水解,利用碳酸钠溶液呈碱性,除去铁表面的油污;加快溶解可通过搅拌或加热实现;
(2)当有晶膜出现时,则停止加热,防止摩尔盐失水;
(3)过滤适用于不溶于水的固体和液体;减压的操作优点是:可加快过滤速度,并能得到较干燥的沉淀;
(4)根据“相似相溶原理”可知摩尔盐易溶于水,难溶于有机溶剂;
(5)①Fe2+→Fe3+,铁元素化合价升高1价;MnO4-+→Mn2+,锰元素降低5价,化合价升降最小公倍数为5,根据得失电子守恒、原子守恒书写方程式;
②根据关系式5Fe2+~MnO4-,计算4g产品中Fe2+的物质的量,进而计算Fe2+的质量,再根据质量分数定义计算.
解答 解:制取摩尔盐晶体流程为:先利用碳酸钠溶液呈碱性,除去铁表面的油污,然后加稀硫酸溶解,铁与稀硫酸反应生成亚铁离子,加入硫酸铵发生(NH4)2 SO4+FeSO4+6H2O=(NH4)2SO4•FeSO4•6H2O↓,结晶过滤,摩尔盐易溶于水,难溶于有机溶剂,用酒精洗涤摩尔盐,得到摩尔盐晶体.
(1)Na2CO3溶液中CO32-水解CO32-+H2O?HCO3-+OH-,使Na2CO3溶液呈碱性,油脂在碱性溶液中水解生成溶于水的物质易于洗去,步骤1中加入10%Na2CO3溶液的主要作用是除去铁屑表面的油污,搅拌、升温都能加快水分子运动速度,也就能加快盐与水的接触机会,从而加快了盐的溶解速率,
故答案为:利用碳酸钠溶液呈碱性,除去铁表面的油污;搅拌或加热;
(2)浓缩结晶摩尔盐时要用小火加热,加热浓缩初期可轻微搅拌,但注意观察晶膜,若有晶膜出现,则停止加热,防止摩尔盐失水;更不能蒸发至干,蒸干时溶液中的杂质离子会被带入晶体中,晶体可能会受热分解或被氧化,
故答案为:加热到溶液表面出现晶膜时;
(3)减压过滤,利用大气压强原理,用减小压力的方法加快过滤的速率,并能得到较干燥的沉淀,
故答案为:得到较干燥的沉淀;
(4)摩尔盐易溶于水,不能用蒸馏水洗涤,但摩尔盐属于无机物难溶于有机物,乙醇易挥发,容易干燥;可用乙醇进行洗涤,洗去晶体表面的液体杂质,
故答案为:除去水分,减少晶体溶解损失;容易干燥;
(5)①测定摩尔盐产品中Fe2+的含量,采用在酸性条件下KMnO4标准液滴定,Fe2+→Fe3+,铁元素化合价升高1价;MnO4-+→Mn2+,锰元素降低5价,化合价升降最小公倍数为5,故Fe2++系数为5,MnO4- 系数为1,根据元素守恒可知Mn2+与Fe3+系数分别为1、5,根据电荷守恒可知缺项为H+,H+其系数为2+3×5-[2×5-1]=8,根据H元素守恒可知H2O系数是4,所以反应离子方程式为5Fe2++MnO4-+8H+=1Mn2++5Fe3++4H2O,
故答案为:5Fe2++MnO4-+8H+=5Fe3++Mn2++4H2O;
②测定摩尔盐产品中Fe2+的含量,采用在酸性条件下KMnO4标准液滴定,反应离子方程式为5Fe2++MnO4-+8H+=1Mn2++5Fe3++4H2O,令4g产品中Fe2+的物质的量为xmol,则:
5Fe2+~~~~~~MnO4-,
5 1
xmol 0.01L×0.2mol/L
所以x=$\frac{0.01×0.2mol/L×5}{1}$=0.01mol,所以4g产品中Fe2+的质量0.01mol×56g/mol=0.56g,所以4g产品中Fe2+的质量分数为$\frac{0.56g}{4g}$×100%=14%,
故答案为:14%.
点评 本题以莫尔盐的制备为载体,考查盐类水解、氧化还原反应、氧化还原反应滴定应用、物质分离提纯等有关实验操作以及在新情境下综合运用知识解决问题的能力.题目难度较大,注意基础知识的全面掌握.

 出彩同步大试卷系列答案
出彩同步大试卷系列答案| A. | 丙烯与丁烯 | B. | 丙烷与丁炔 | C. | 乙烯与乙炔 | D. | 乙烷与丙烯 |
| A. | 0.4mol/L | B. | 0.2mol/L | C. | 0.1mol/L | D. | 0.08mol/L |
过程Ⅰ:
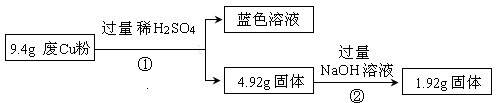
(1)废Cu粉中一定含有的杂质是Fe2O3、SiO2(填化学式)
(2)写出过程②发生反应的离子方程式:SiO2+2OH-═SiO32-+H2O.
过程Ⅱ:
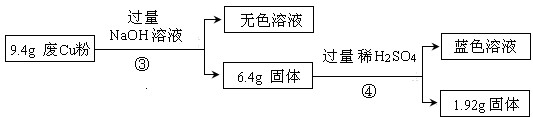
(3)综合过程Ⅰ、II,计算废Cu粉中各成分的质量之比是m(Fe2O3):m(Cu):m(SiO2)=16:16:15(化为最简整数比)
过程Ⅲ:已知25℃时:
| 电解质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 溶度积(Ksp) | 2.2×10-20 | 8.0×10-16 | 4.0×10-38 |
| 开始沉淀时的pH | 5.4 | 6.5 | 3.5 |
| 完全沉淀时的pH | 6.4 | 9.6 | 4.0 |
(5)下列与Ⅲ方案 相关的叙述中,正确的是ACD填字母).
A.H2O2是绿色氧化剂,在氧化过程中不引进杂质、不产生污染
B.将Fe2+氧化为Fe3+的主要原因是Fe(OH)2沉淀比Fe(OH)3沉淀较难过滤
C.调节溶液pH选择的试剂可以是氢氧化铜或氧化铜
D.在pH>4的溶液中Fe3+一定不能大量存在.
| A. | Na2S溶液:c(Na+)>c(HS-)>c(OH-)>c (H2S) | |
| B. | Na2C2O4溶液:c (OH-)=c(H+)+c(HC2O4-)+2c (H2C2O4) | |
| C. | Na2CO3溶液:c (Na+)+c (H+)=2c (CO32-)+c (OH-) | |
| D. | CH3COONa和CaCl2混合溶液:c (Na+)+c (Ca2+)=c (CH3COO-)+c (CH3COOH)+2c (Cl-) |
| A. | 在该反应中,每生成0.1mol氧气转移0.2mol电子 | |
| B. | Na、Na2O2中钠元素微粒的半径:r(Na)<r(Na+) | |
| C. | 元素氧的单质只存在氧气和臭氧两种同素异形体 | |
| D. | 在该反应条件下,氧元素的非金属性强于碳元素的非金属性 |
 不能氧化为氧化成醛或酸
不能氧化为氧化成醛或酸
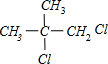 PMAA
PMAA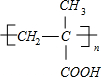
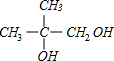 +O2$→_{△}^{Cu}$2
+O2$→_{△}^{Cu}$2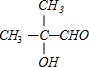 +2H2O;
+2H2O; $→_{△}^{浓硫酸}$CH2=C(CH3)-COOH+H2O.
$→_{△}^{浓硫酸}$CH2=C(CH3)-COOH+H2O.