题目内容
2.为了将混有K2SO4、MgSO4、CaCl2的KCl固体提纯,并制得纯净的KCl晶体,某同学设计如下实验方案: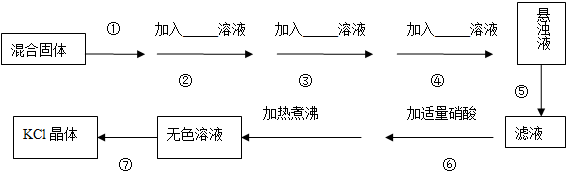
(1)操作①⑤⑦的名称依次是溶解、过滤、蒸发
(2)操作②~④加入的试剂可以为BaCl2、KOH、K2CO3或KOH、BaCl2、K2CO3或BaCl2、K2CO3、KOH.
(3)实验过程中产生的多次沉淀不需要(填“需要”或“不需要”)多次过滤,理由是生成的沉淀可一次性过滤,如果多次过滤会使过程复杂化.
(4)该同学设计的实验方案不严密(填“严密”或“不严密”),理由是第⑥步加硝酸会引入杂质NO3-.该步骤所加试剂及其作用是应加盐酸调节pH,除去过量的KOH、K2CO3.
分析 由实验流程可知,除去SO42-、Ca2+、Mg2+离子的方法一般是使它们分别形成BaSO4、CaCO3、Mg(OH)2沉淀,所以需要加入稍过量的BaCl2K2CO3、KOH溶液,过量的Ba2+可用K2CO3溶液除去,因此实验时必须先加入Ba(NO3)2溶液,后加入K2CO3溶液,则试剂顺序为BaCl2、KOH、K2CO3或KOH、BaCl2、K2CO3或BaCl2、K2CO3、KOH,操作①为溶解,⑤为过滤,⑥应加稀盐酸调节溶液的pH,否则会引入杂质,⑦为蒸发结晶得到KCl,以此来解答.
解答 解:由实验流程可知,除去SO42-、Ca2+、Mg2+离子的方法一般是使它们分别形成BaSO4、CaCO3、Mg(OH)2沉淀,所以需要加入稍过量的BaCl2K2CO3、KOH溶液,过量的Ba2+可用K2CO3溶液除去,因此实验时必须先加入Ba(NO3)2溶液,后加入K2CO3溶液,则试剂顺序为BaCl2、KOH、K2CO3或KOH、BaCl2、K2CO3或BaCl2、K2CO3、KOH,操作①为溶解,⑤为过滤,⑥应加稀盐酸调节溶液的pH,否则会引入杂质,⑦为蒸发结晶得到KCl,
(1)由上述分析可知,操作①⑤⑦的名称依次是溶解、过滤、蒸发,故答案为:溶解、过滤、蒸发;
(2)操作②~④加入的试剂可以为BaCl2、KOH、K2CO3或KOH、BaCl2、K2CO3或BaCl2、K2CO3、KOH,
故答案为:BaCl2、KOH、K2CO3或KOH、BaCl2、K2CO3或BaCl2、K2CO3、KOH;
(3)为简化实验操作,可一次性过滤,如果多次过滤会使过程复杂化,则不需要多次过滤,故答案为:不需要;生成的沉淀可一次性过滤,如果多次过滤会使过程复杂化;
(4)由上述分析可知,不能利用硝酸调节pH,应加盐酸调节pH,除去过量的KOH、K2CO3,则实验不严密,故答案为:不严密;第⑥步加硝酸会引入杂质NO3-;应加盐酸调节pH,除去过量的KOH、K2CO3.
点评 本题考查混合物的分离提纯的综合应用,为高频考点,把握流程中的反应、混合物分离方法选择为解答的关键,侧重分析与实验能力的考查,题目难度不大.

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案| A. | K+、MnO4-、Na+、Cl- | B. | Na+、Cl-、NO3-、SO42- | ||
| C. | K+、Na+、NO3-、HCO3- | D. | Fe3+、Na+、CO32-、SO42- |
| A. | 浊液 | B. | 溶液 | C. | 纯净物 | D. | 胶体 |
| A. | 从1L1mol/L的氯化钠溶液中取出10ml,其浓度仍是1mol/L | |
| B. | 将80 g NaOH溶于1 L水中,所得溶液中NaOH的物质的量浓度为2 mol/L | |
| C. | 0.5 L 2mol/L的氯化钡溶液中,钡离子和氯离子总数约为3×6.02×1023 | |
| D. | 10g 98%硫酸(密度为1.84g/cm3)与10mL18.4mol/L硫酸的物质的量浓度是相同的 |
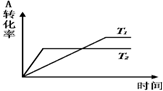
| A. | T1>T2,正反应是吸热反应 | B. | T1<T2,正反应是放热反应 | ||
| C. | T1<T2,正反应是吸热反应 | D. | T1>T2,正反应是放热反应 |
| A. | 加稀盐酸后过滤,除去混在铜粉中的少量镁粉和铝粉 | |
| B. | 用BaCl2除去NaOH溶液中混有的少量Na2SO4 | |
| C. | 将O2和H2的混合气体通过灼热的氧化铜,以除去其中的H2 | |
| D. | 用溶解、过滤的方法分离CaCl2和NaCl固体混合物 |
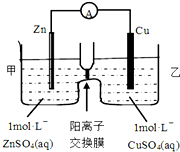 为充分利用海洋资源,研究人员发明海水电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列说法错误的是( )
为充分利用海洋资源,研究人员发明海水电池,这种电池能利用淡水与海水之间含盐量差别进行发电,在海水中电池总反应可表示为:5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl,下列说法错误的是( )| A. | 负极反应式:Ag+Cl-e-=AgCl | |
| B. | 每生成1 mol Na2Mn5O10转移2 mol电子 | |
| C. | Na2Mn5O10是还原产物 | |
| D. | Cl-不断向电池的正极移动 |