题目内容
10.乙醛是一种重要的化工产品,在一定条件下能被氧化成乙酸.A、B、C、D、E为有机物,以乙烯为原料,生产各有机物的转化关系如图所示(部分产物和反应条件已略去).
请回答下列问题:
(1)A的结构简式为-[--CH2--CH2--]n-;
(2)B+D→E的反应类型为酯化反应(或取代反应);
(3)CH2=CH2和H2O在一定条件下反应生成B的化学方程式为_CH2=CH2+H2O一定条件下→CH3CH2OH.
分析 CH2=CH2,乙烯含有碳碳双键,可发生加聚反应生成聚乙烯A为-[--CH2--CH2--]n-,乙烯与水发生加成反应得到B为CH3CH2OH,B发生催化氧化生成C为CH3CHO,C进一步发生氧化反应生成D为CH3COOH,乙醇与乙酸发生酯化反应得到乙酸乙酯,据此解答.
解答 解:CH2=CH2,乙烯含有碳碳双键,可发生加聚反应生成聚乙烯A为-[--CH2--CH2--]n-,乙烯与水发生加成反应得到B为CH3CH2OH,B发生催化氧化生成C为CH3CHO,C进一步发生氧化反应生成D为CH3COOH,乙醇与乙酸发生酯化反应得到乙酸乙酯,
(1)乙烯含有碳碳双键,可发生加聚反应生成聚乙烯A为)--[--CH2--CH2--]n-,故答案为:--[--CH2--CH2--]n-;
(2)乙醇与乙酸发生酯化反应得到乙酸乙酯,故答案为:酯化反应(或取代反应);
(3)CH2=CH2和H2O在一定条件下反应生成乙醇的化学方程式为CH2=CH2+H2O一定条件下→CH3CH2OH,故答案为:CH2=CH2+H2O一定条件下→CH3CH2OH.
点评 本题考查有机物的推断,涉及烯、醇、醛、羧酸等的性质与转化等,难度不大,注意对基础知识的理解掌握.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
20.已知A(g)+B(g)═C(g)+D(g)反应的平衡常数和温度的关系如下:
回答下列问题:
①该反应的平衡常数表达式K=c(C)×c(D)c(A)×c(B),△H>0(填“<”、“>”或“=”);
②830℃时,向一个5L的密闭容器中充入0.20mol的A和0.60mol的B,若反应经一段时间后,达到平衡时A的转化率为75%.如果这时向该密闭容器中再充入1molA气体,平衡向右移动(填“左”、“右”或“不移动”).平衡时A的转化率减小;(填“增大”、“减小”或“不变”).
| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常数 | 0.4 | 0.6 | 1.0 | 1.1 | 1.6 |
①该反应的平衡常数表达式K=c(C)×c(D)c(A)×c(B),△H>0(填“<”、“>”或“=”);
②830℃时,向一个5L的密闭容器中充入0.20mol的A和0.60mol的B,若反应经一段时间后,达到平衡时A的转化率为75%.如果这时向该密闭容器中再充入1molA气体,平衡向右移动(填“左”、“右”或“不移动”).平衡时A的转化率减小;(填“增大”、“减小”或“不变”).
1.下列各组离子在溶液中能大量共存的是( )
| A. | Na+、Mg2+、Cl-、OH- | B. | SO32-、SO42-、H+、K+ | ||
| C. | Fe2+、Fe3+、Cu2+、Cl- | D. | Ba2+、Na+、SO42-、Cl- |
18.原电池工作时能量转化的主要形式是( )
| A. | 化学能转化为电能 | B. | 电能转化为化学能 | ||
| C. | 化学能转化为热能 | D. | 化学能转化为光能 |
5.了解用药常识,有利于自我保健.下列药物使用正确的是( )
| A. | 阿司匹林课解热镇痛,常用于治疗感冒 | |
| B. | 氢氧化钠能中和胃酸,可用于治疗胃酸过多 | |
| C. | 蚕丝的主要成分是纤维素 | |
| D. | 合金中一定只含金属元素 |
15.下列常用实验仪器中,能直接加热的是( )
| A. | 分液漏斗 | B. | 普通漏斗 | C. | 蒸馏烧瓶 | D. | 蒸发皿 |
20.下列有关反应:4NH3(g)+5O2(g)═4NO(g)+6H2O(g)△H (298K)=-905kJ•mol-1 的描述不正确的是( )
| A. | 生成物的总能量小于反应物的总能量 | |
| B. | 该反应的燃烧热为905KJ | |
| C. | 该反应为放热反应 | |
| D. | 该反应中每4molNH3(g)被氧化,放出905 kJ热量 |


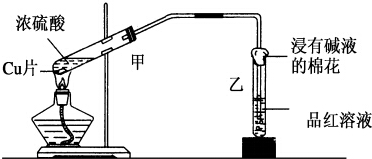 实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验.
实验室常用下列装置来进行铜跟浓硫酸反应等一系列实验.