题目内容
12.在酸性溶液中能大量共存且溶液为无色透明的离子组是( )| A. | K+、MnO4-、Na+、Cl- | B. | Na+、Cl-、NO3-、SO42- | ||
| C. | K+、Na+、NO3-、HCO3- | D. | Fe3+、Na+、CO32-、SO42- |
分析 溶液无色时可排除Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,酸性溶液中存在大量氢离子,
A.高锰酸根离子为有色离子,且酸性条件下高锰酸根离子能够氧化氯离子;
B.四种离子之间不反应,都不与氢离子反应,且为无色溶液;
C.碳酸氢根离子与氢离子反应;
D.铁离子为有色离子,铁离子与碳酸根离子发生双水解反应.
解答 解:无色溶液时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在,酸性溶液中存在大量氢离子,
A.MnO4-为有色离子,且在酸性条件下MnO4-、Cl-之间发生氧化还原反应,在溶液中不能大量共存,故A错误;
B.Na+、Cl-、NO3-、SO42-之间不反应,都是无色离子,都不与氢离子反应,在溶液中能够大量共存,故B正确;
C.HCO3-与氢离子反应生成二氧化碳气体,在溶液中不能大量共存,故C错误;
D.Fe3+为有色离子,Fe3+、CO32-之间发生水解反应生成氢氧化铁沉淀和二氧化碳气体,在溶液中不能大量共存,故D错误;
故选B.
点评 本题考查离子共存的判断,为高考的高频题,属于中等难度的试题,注意明确离子不能大量共存的一般情况:能发生复分解反应的离子之间; 能发生氧化还原反应的离子之间等;还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的颜色,如无色时可排除 Cu2+、Fe2+、Fe3+、MnO4-等有色离子的存在.

练习册系列答案
相关题目
2.反应4A(g)+5B(g)═4C(g)+6D(g),在5L的密闭容器中进行,半分钟后,C的物质的量增加了0.30mol.下列叙述正确的是( )
| A. | 容器中含D物质的量至少为0.45 mol | |
| B. | A的平均反应速率是0.010 mol•L-1•s-1 | |
| C. | 容器中A、B、C、D的物质的量之比一定是4:5:4:6 | |
| D. | 容器中A的物质的量一定增加了0.30 mol |
3.由两种烃组成的混合气体2L与足量的氧气充分反应后生成5LCO2、6LH2O(所有体积都在120℃测定),则这两种混合气体的可能组成是( )
| A. | C2H4、C3H8 | B. | CH4、C3H8 | C. | CH4、C4H10 | D. | C2H2、C3H8 |
20.已知A(g)+B(g)═C(g)+D(g)反应的平衡常数和温度的关系如下:
回答下列问题:
①该反应的平衡常数表达式K=$\frac{c(C)×c(D)}{c(A)×c(B)}$,△H>0(填“<”、“>”或“=”);
②830℃时,向一个5L的密闭容器中充入0.20mol的A和0.60mol的B,若反应经一段时间后,达到平衡时A的转化率为75%.如果这时向该密闭容器中再充入1molA气体,平衡向右移动(填“左”、“右”或“不移动”).平衡时A的转化率减小;(填“增大”、“减小”或“不变”).
| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常数 | 0.4 | 0.6 | 1.0 | 1.1 | 1.6 |
①该反应的平衡常数表达式K=$\frac{c(C)×c(D)}{c(A)×c(B)}$,△H>0(填“<”、“>”或“=”);
②830℃时,向一个5L的密闭容器中充入0.20mol的A和0.60mol的B,若反应经一段时间后,达到平衡时A的转化率为75%.如果这时向该密闭容器中再充入1molA气体,平衡向右移动(填“左”、“右”或“不移动”).平衡时A的转化率减小;(填“增大”、“减小”或“不变”).
7.下列有关元素周期表的叙述正确的是( )
| A. | 同周期主族元素,原子半径随原子序数增大而增大 | |
| B. | 第3周期主族元素的最高正化合价等于它所处的主族序数 | |
| C. | 周期表中所含元素种类最多的族是ⅠA族 | |
| D. | 稀有气体元素原子的最外层电子数均为8 |
17.如图图示装置的实验中,操作正确的是( )
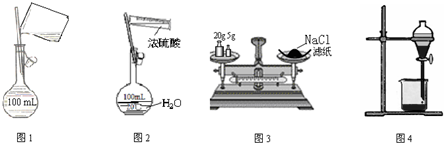

| A. | 图1配制250mL0.10mol•L-1盐酸 | B. | 图2稀释浓硫酸 | ||
| C. | 图3称量氯化钠固体 | D. | 图4CCl4萃取碘水的分液操作 |
1.下列各组离子在溶液中能大量共存的是( )
| A. | Na+、Mg2+、Cl-、OH- | B. | SO32-、SO42-、H+、K+ | ||
| C. | Fe2+、Fe3+、Cu2+、Cl- | D. | Ba2+、Na+、SO42-、Cl- |