题目内容
【题目】下表列出了①~⑨九种元素在周期表中的位置。
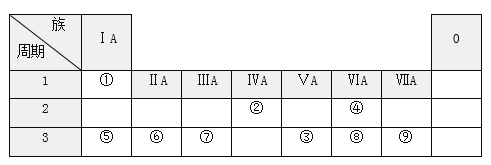
请按要求回答下列问题:
(1)元素⑦的原子结构示意图______________________。①、④按原子个数比为1:1组成的分子的电子式____________________;由②、④两种元素组成的一种化合物的结构式________________;
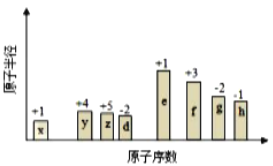
(2)⑤⑥两种元素的原子半径由大到小的顺序是____________(填元素符号)。
(3)⑧和⑨两种元素的最高价氧化物对应的水化物中酸性较弱的是________(填化学式)。
(4)元素③的气态氢化物和元素⑧的气态氢化物易于制备的是___________(填化学式)。
(5)元素⑤的最高价氧化物对应的水化物与元素⑦的最高价氧化物对应水化物反应,其离子方程式为_________________________________________。
(6)元素①、④、⑤两两之间可以形成两种类型的化合物,写出一种共价化合物的化学式__________________ ;一种离子化合物的化学式_________。
【答案】![]()
![]() O=C=O Na>Mg H2SO4 H2S Al(OH)3+OH-=AlO2-+2H2O H2O Na2O
O=C=O Na>Mg H2SO4 H2S Al(OH)3+OH-=AlO2-+2H2O H2O Na2O
【解析】
根据元素在周期表中的位置知①②③④⑤⑥⑦⑧⑨分别是H、C、P、O、Na、Mg、Al、S、Cl元素。
(1) 元素⑦为Al,原子结构示意图为:![]() ;①、④按原子个数比为1:1组成的分子为:H2O2,电子式为:
;①、④按原子个数比为1:1组成的分子为:H2O2,电子式为:![]() ;由②、④两种元素组成的化合物为:CO2, 结构式为:O=C=O。答案为:
;由②、④两种元素组成的化合物为:CO2, 结构式为:O=C=O。答案为: 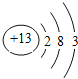 ;
;![]() ;O=C=O;
;O=C=O;
(2)Na与Mg均属于同种周期元素,由于核电核数Na![]() Mg,故半径Na
Mg,故半径Na![]() Mg,因此,答案为: Na>Mg;
Mg,因此,答案为: Na>Mg;
(3)因为非金属性Cl![]() S,故酸性:高氯酸大于硫酸,答案为: H2SO4 ;
S,故酸性:高氯酸大于硫酸,答案为: H2SO4 ;
(4)因为非金属性S>P,故H2S更易制备,因此,答案为: H2S;
(5)氢氧化铝与氢氧化钠反应生成偏铝酸钠和水,氢氧化铝难溶,不能拆,水为氧化物不能拆,离子反应方程式为: Al(OH)3+OH-=AlO2-+2H2O,答案为: Al(OH)3+OH-=AlO2-+2H2O;
(6)H、O和Na形成的共价化合物为水,离子化合物为过氧化钠、氧化钠、氢氧化钠等,答案为: H2O、Na2O

【题目】在一定温度下,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应:X(g)+Y(g) ![]() 2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法不正确的是
2Z(g)△H<0,一段时间后达到平衡,反应过程中测定的数据如下表:下列说法不正确的是
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
A. 反应前2min的平均速率v(Z)=2.0×10-3 mol·L-1·min-1
B. 其他条件不变,降低温度,反应达到新平衡前:v(逆)<v(正)
C. 该温度下此反应的平衡常数:K=1.44
D. 保持其他条件不变,起始时向容器充入0.32 mol气体X和0.32 mol气体Y,到达平衡时,c(Z)=0.024 mol/L