��Ŀ����
17��X��Y��Z��W��Q��R��Ϊǰ������Ԫ�أ���ԭ��������������XԪ�ص�ԭ�ӵİ뾶������ԭ�Ӱ뾶����С��YԪ�صĻ�̬ԭ���е��ӷֲ���������ͬ���ܼ��У���ÿ���ܼ��еĵ���������ͬ��ZԪ�ص���̬�⻯����������������Ӧ��ˮ�����ܷ������Ϸ�Ӧ��WԪ�ص�������������������������QΪǰ�������е縺����С��Ԫ�أ�RԪ�ص�ԭ�Ӻ����11��������гɶԵ��ӣ���ش��������⣺���þ���Ļ�ѧ����ش�
��1��YԪ�صĻ�̬ԭ�ӵĵ����Ų�ʽΪ1s22s22p2��Z��WԪ��ԭ�ӵ�һ�����ܽϴ����N��RԪ�������ڱ�������d����
��2��XYZ�ĵ���ʽΪ
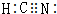 ������Yԭ�ӵ��ӻ���ʽ��sp��ZW3-�Ŀռ乹��Ϊƽ�������Σ�
������Yԭ�ӵ��ӻ���ʽ��sp��ZW3-�Ŀռ乹��Ϊƽ�������Σ���3��X��Y��W��Q����Ԫ������������Ԫ�ؿ��γ����ֻ�������ң�������ˮ��Һ���ʼ��ԣ����ܴٽ�ˮ�ĵ��룬��������ˮ�ĵ��룬���ˮ��Һ������Ũ���ɴ�С��˳��Ϊc��K+����c��CO32-����c��OH-����c ��HCO3-����c��H+���������£������ҵ�ˮ��Һ��pH��Ϊ11��������Һ��ˮ�����c��OH-��֮��Ϊ���ף��ң�108��1��
��4��ZX3��������NaOH��Һ�����¿ɹ��ɸ���ȼ�ϵ�أ����ɵIJ���Ի�������Ⱦ���õ�صĸ�����ӦΪ2NH3-6e-+6OH-=N2+6H2O��
��5��RW42-����ǿ�����ԣ���ϡ������Һ�о��ҷ�Ӧ���õ�һ����ɫ����ͻ�ɫ��Һ���÷�Ӧ�����ӷ���ʽ��4FeO42-+20 H+=4Fe3++3O2��+10H2O��
���� X��Y��Z��W��Q��R��Ϊǰ������Ԫ�أ���ԭ��������������XԪ�ص�ԭ�ӵİ뾶������ԭ�Ӱ뾶����С����XΪHԪ�أ�YԪ�صĻ�̬ԭ���е��ӷֲ���������ͬ���ܼ��У���ÿ���ܼ��еĵ���������ͬ��ԭ�Ӻ�������Ų�Ϊ1s22s22p2����YΪCԪ�أ�ZԪ�ص���̬�⻯����������������Ӧ��ˮ�����ܷ������Ϸ�Ӧ����ZΪNԪ�أ�WԪ�ص�������������������������ԭ��ֻ�ܴ��ڵڶ����ڣ���WΪOԪ�أ�QΪǰ�������е縺����С��Ԫ�أ���QΪNa��RԪ�ص�ԭ�Ӻ����11��������гɶԵ��ӣ���������Ų�Ϊ1s22s22p63s23p23d64s2����RΪFe���ݴ˽��
��� �⣺X��Y��Z��W��Q��R��Ϊǰ������Ԫ�أ���ԭ��������������XԪ�ص�ԭ�ӵİ뾶������ԭ�Ӱ뾶����С����XΪHԪ�أ�YԪ�صĻ�̬ԭ���е��ӷֲ���������ͬ���ܼ��У���ÿ���ܼ��еĵ���������ͬ��ԭ�Ӻ�������Ų�Ϊ1s22s22p2����YΪCԪ�أ�ZԪ�ص���̬�⻯����������������Ӧ��ˮ�����ܷ������Ϸ�Ӧ����ZΪNԪ�أ�WԪ�ص�������������������������ԭ��ֻ�ܴ��ڵڶ����ڣ���WΪOԪ�أ�QΪǰ�������е縺����С��Ԫ�أ���QΪNa��RԪ�ص�ԭ�Ӻ����11��������гɶԵ��ӣ���������Ų�Ϊ1s22s22p63s23p23d64s2����RΪFe��
��1��YԪ�صĻ�̬ԭ���е��ӷֲ���������ͬ���ܼ��У���ÿ���ܼ��еĵ���������ͬ��ԭ�Ӻ�������Ų�Ϊ1s22s22p2��ZΪNԪ�ء�WΪOԪ�أ�NԪ��ԭ��2p�ܼ�����3�����ӣ�Ϊ�����ȶ�״̬�������ϵͣ���һ�����ܸ�����Ԫ�أ�RΪFeԪ�أ������ڱ���λ������d����
�ʴ�Ϊ��1s22s22p2��N��d��
��2��XYZΪHCN������ʽΪ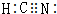 ������Cԭ�ӵ��ӻ���ʽ��sp�ӻ���NO3-��Nԭ�ӹµ��Ӷ���Ϊ$\frac{5+1-2��3}{2}$=0���۲���Ӷ���Ϊ3+0=3����ռ乹��Ϊ��ƽ�������Σ�
������Cԭ�ӵ��ӻ���ʽ��sp�ӻ���NO3-��Nԭ�ӹµ��Ӷ���Ϊ$\frac{5+1-2��3}{2}$=0���۲���Ӷ���Ϊ3+0=3����ռ乹��Ϊ��ƽ�������Σ�
�ʴ�Ϊ��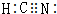 ��sp��ƽ�������Σ�
��sp��ƽ�������Σ�
��3��H��C��O��Na����Ԫ������������Ԫ�ؿ��γ����ֻ�������ң�������ˮ��Һ���ʼ��ԣ����ܴٽ�ˮ�ĵ��룬��������ˮ�ĵ��룬���ΪNa2CO3�ȡ���ΪNaOH��
Na2CO3��ˮ��Һ��̼���ˮ�⣬��Һ�ʼ��ԣ���Һ������������Դ��̼���ˮ����ˮ�ĵ��룬��c��OH-����c ��HCO3-��������Һ������Ũ���ɴ�С��˳��Ϊ��c��K+����c��CO32-����c��OH-����c ��HCO3-����c��H+����
�����£������ҵ�ˮ��Һ��pH��Ϊ11��̼������Һ������������ȫ��Դ��ˮ�������Һ��ˮ�����c��OH-��=$\frac{1{0}^{-14}}{1{0}^{-11}}$=10-3mol/L���������Ʒ�Ӧ��ˮ��������������ӵ�����Һ��������Ũ�ȣ�������������Һ��ˮ�����c��OH-��=10-11mol/L��������Һ��ˮ�����c��OH-��֮��Ϊ10-3mol/L��10-11mol/L=108��1��
�ʴ�Ϊ��c��K+����c��CO32-����c��OH-����c ��HCO3-����c��H+����108��1��
��4��NH3��������NaOH��Һ�����¿ɹ��ɸ���ȼ�ϵ�أ����ɵIJ���Ի�������Ⱦ��������Ӧ���ɵ�����ˮ����������������Ӧ�������ٸ���ʧȥ���ӣ��������������ɵ�����ˮ���õ�صĸ�����ӦΪ��2NH3-6e-+6OH-=N2+6H2O��
�ʴ�Ϊ��2NH3-6e-+6OH-=N2+6H2O��
��5��FeO42-����ǿ�����ԣ���ϡ������Һ�о��ҷ�Ӧ���õ�һ����ɫ����ͻ�ɫ��Һ����Ӧ�������������������÷�Ӧ�����ӷ���ʽ�ǣ�4FeO42-+20 H+=4Fe3++3O2��+10H2O��
�ʴ�Ϊ��4FeO42-+20 H+=4Fe3++3O2��+10H2O��
���� ���⿼��ṹ����λ�ù�ϵӦ�ã��漰��������Ų�������ʽ���ӻ���ʽ���������жϡ������ܡ�����ˮ�⡢ԭ��ء�������ԭ��Ӧ�ȣ��Ƕ�ѧ���ۺ������Ŀ��飬�Ѷ��еȣ�

 ��ҵ����ϵ�д�
��ҵ����ϵ�д� ͬ��ѧ��һ�ζ���ϵ�д�
ͬ��ѧ��һ�ζ���ϵ�д�| A�� | �����л��߷��Ӳ��� | B�� | ����ʹ�û��������ɫ��Ⱦ�� | ||
| C�� | ����ԭ�����ϡ���ɫ��ѧ��˼�� | D�� | ��ҵ��ͨ������Ӿۺϳ� |
| A�� | 2AgNO3+MgCl2�T2AgCl��+Mg��NO3��2 | B�� | K2CO3+Ca��OH��2�TCaCO3��+2KOH | ||
| C�� | CaCl2+CO2+H2O�TCaCO3��+2HCl | D�� | HCl+KOH�TKCl+H2O |
| A�� | FeCl2��Һ��ͨ��Cl2��Fe2++Cl2=Fe3++2Cl- | |
| B�� | ����ʯ��ˮ������С�մ���Һ��ϣ�Ca2++OH-+HCO3-=CaCO3��+H2O | |
| C�� | ��������������������Һ Al+2OH-=AlO2-+H2�� | |
| D�� | AlCl3��Һ�м��������ˮ��Al3++4OH-=AlO2-+2H2O |
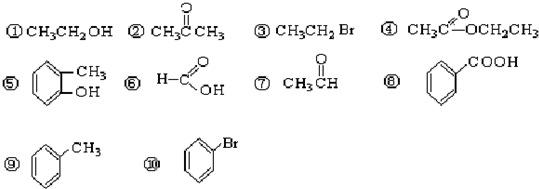
| A�� | CH2Br-CH2Br | B�� | C5H11OH | C�� | C100H202 | D�� | C6H6 |
C��ʯī��+$\frac{1}{2}$O2��g���TCO��g����H=-111kJ/mol
H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=-242kJ/mol
C��ʯī��+O2��g���TCO2��g����H=-394kJ/mol
��25��ʱ1mol CO��ˮ��������ת��Ϊ�����Ͷ�����̼��Ӧ��HΪ��������
| A�� | +41��kJ/mol | B�� | -41kJ/mol | C�� | 283kJ/mol | D�� | -131kJ/mol |
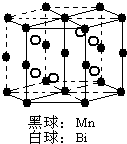 ����������λ�����ڱ��ڢ�A�壬���ǵĵ��ʼ��仯��������������������й㷺Ӧ�ã���ش��й����⣺
����������λ�����ڱ��ڢ�A�壬���ǵĵ��ʼ��仯��������������������й㷺Ӧ�ã���ش��й����⣺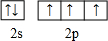 ��
��